Organiske syrer:Forståelse af styrke og egenskaber
Her er hvorfor:
* Svage syrer ioniser ikke fuldstændigt i opløsning. De donerer kun delvist deres brintioner (H+).
* Stærke syrer ionisere på den anden side fuldstændigt i opløsning.
Eksempler på organiske syrer:
* Carboxylsyrer: Disse er den mest almindelige type organisk syre med den generelle formel R-COOH, hvor R er en carbonhydridgruppe. Eksempler omfatter eddikesyre (CH3COOH), myresyre (HCOOH) og citronsyre (C6H8O7).
* Sulfonsyrer: Disse har den almene formel R-SO3H, hvor R er en carbonhydridgruppe. Eksempler omfatter methansulfonsyre (CH3SO3H).
* Fenoler: Disse er aromatiske forbindelser med en hydroxylgruppe (OH) knyttet til den aromatiske ring.
Hvorfor er organiske syrer svage?
* Tilstedeværelsen af carbonhydridgruppen: Kulbrintegruppen knyttet til den sure funktionelle gruppe (som COOH eller SO3H) er elektrondonerende. Dette gør hydrogenionen mindre tilbøjelig til at dissociere fra molekylet, hvilket resulterer i svagere surhedsgrad.
* Induktiv effekt: Den elektrondonerende effekt af kulbrintegruppen kan forstærkes yderligere af den induktive effekt, hvor elektroner skubbes mod den sure funktionelle gruppe.
* Resonans: Nogle organiske syrer, som carboxylsyrer, kan udvise resonansstrukturer, der delokaliserer den negative ladning dannet efter tabet af en proton. Denne stabilisering af konjugatbasen gør syren svagere.
Vigtig bemærkning: Der er nogle organiske syrer, der anses for stærkere end andre. For eksempel er trifluoreddikesyre (CF3COOH) en stærk organisk syre på grund af fluoratomernes elektrontiltrækkende virkning.
 Varme artikler
Varme artikler
-
 Solcellemateriale klarer sig bedre under trykAdskillelse af bromid og iodid i perovskitter resulterer i et inhomogent energilandskab, afbildet som bakker og dale. Ved højt tryk, jodidet og bromidet forbliver homogent fordelt, så perovskitterne b
Solcellemateriale klarer sig bedre under trykAdskillelse af bromid og iodid i perovskitter resulterer i et inhomogent energilandskab, afbildet som bakker og dale. Ved højt tryk, jodidet og bromidet forbliver homogent fordelt, så perovskitterne b -
 Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt
Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt -
 En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner
En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner -
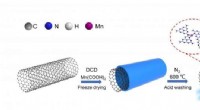 Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne
Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne
- Hvilket domæne inkluderer kun organismer med en kerne i deres celler?
- Hvornår har en hoppekugle mindst potentiel energi?
- Kæmpe bor, der bruges til at tunnelere gennem bjerge?
- Hvilke typer deformation gennemgår klipper under dannelse af et orogen bælte, såsom Alperne?
- Designerproteiner danner ledninger og gitter på mineraloverfladen
- Skal NASA til Mars? Eller månen? Eller ingen steder?


