Calciumchlorid:Forståelse af ioniske bindinger og kemisk struktur
* Elektrostatisk tiltrækning: Calcium (Ca) er et metal og har en tendens til at miste to elektroner for at danne en positiv ion (Ca²⁺). Klor (Cl) er et ikke-metal og har en tendens til at få en elektron til at danne en negativ ion (Cl⁻). Den stærke elektrostatiske tiltrækning mellem de positivt ladede calciumioner og de negativt ladede chloridioner danner ionbindingen.
* Elektronegativitetsforskel: Elektronegativitetsforskellen mellem calcium (1,0) og klor (3,0) er stor (2,0), hvilket indikerer en overførsel af elektroner i stedet for deling.
* Struktur: Ioniske forbindelser danner typisk krystallinske strukturer på grund af det regelmæssige arrangement af ioner i et gitter. Calciumchlorid danner et krystalgitter med calciumioner omgivet af chloridioner.
Opsummering: Den store elektronegativitetsforskel, dannelsen af ioner og krystalstrukturen peger alle mod en ionbinding i calciumchlorid.
 Varme artikler
Varme artikler
-
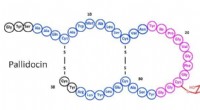 Nyt potent antimikrobielt middel fra termofil bakterieStrukturen af pallidocin, cirkler er aminosyreresterne, det funktionelle sukker ses til højre, knyttet til Cys. Kredit:Oscar Kuipers / University of Groningen Mikrobiologer fra University of Gro
Nyt potent antimikrobielt middel fra termofil bakterieStrukturen af pallidocin, cirkler er aminosyreresterne, det funktionelle sukker ses til højre, knyttet til Cys. Kredit:Oscar Kuipers / University of Groningen Mikrobiologer fra University of Gro -
 Forskere designer et enzym til at syntetisere kulhydraterKredit:Universidad de Barcelona Sukker- eller kulhydratsyntese er vigtig for udviklingen af diagnostiske tests, vacciner og nye lægemidler. I en samarbejdsundersøgelse, forskere har syntetiseret
Forskere designer et enzym til at syntetisere kulhydraterKredit:Universidad de Barcelona Sukker- eller kulhydratsyntese er vigtig for udviklingen af diagnostiske tests, vacciner og nye lægemidler. I en samarbejdsundersøgelse, forskere har syntetiseret -
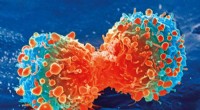 Forskere bruger katalysatorer til at ødelægge kræftceller indefraKræftcelle under celledeling. Kredit:National Institutes of Health At bruge trojanske heste til at bekæmpe kræft inde fra selve tumorcellerne uden at beskadige sundt væv er formålet med dette nye
Forskere bruger katalysatorer til at ødelægge kræftceller indefraKræftcelle under celledeling. Kredit:National Institutes of Health At bruge trojanske heste til at bekæmpe kræft inde fra selve tumorcellerne uden at beskadige sundt væv er formålet med dette nye -
 Forskere afslører dynamikken mellem klynger og klynger mellem thiolatbeskyttede guld-sølvlegeringe…Kredit:CC0 Public Domain Fra effektiv medicin til molekylære sensorer til brændselsceller, metalklynger bliver grundlæggende nyttige i sundheden, miljø, og energisektorer. Denne forskelligartede f
Forskere afslører dynamikken mellem klynger og klynger mellem thiolatbeskyttede guld-sølvlegeringe…Kredit:CC0 Public Domain Fra effektiv medicin til molekylære sensorer til brændselsceller, metalklynger bliver grundlæggende nyttige i sundheden, miljø, og energisektorer. Denne forskelligartede f
- Hvilket væv gemmer energi?
- Hvornår blev teorien om relativitet først foreslået?
- Hvad er en fordel ved geotermisk energi frem for vindenergi?
- Er det sikkert at fodre opdrættet laks med børsteorme opdrættet på fiskeekskrementer?
- Hvilken planet har den varmeste overskyede planet?
- Hvad spiser en prokaryote?


