Hvorfor er bor en metalloid i gruppe 13? - Det periodiske system forklaret
Her er forklaringen:
* Elektronisk konfiguration: Alle grundstoffer i gruppe 3A har 3 valenselektroner (elektroner i deres yderste skal). Dette er gruppens definerende karakteristika. Boron har den elektroniske konfiguration af 2s²2p¹, ligesom de andre medlemmer af gruppen.
* Lignende kemisk adfærd: Mens Borons kemiske adfærd adskiller sig i nogle aspekter fra resten af gruppen, deler den ligheder i visse reaktioner. For eksempel kan bor danne forbindelser med en +3 oxidationstilstand, svarende til andre grundstoffer i gruppen.
Men hvorfor er bor anderledes?
Bor er et mindre atom sammenlignet med de andre grundstoffer i gruppen. Dette resulterer i:
* Stærkere tiltrækning mellem kernen og elektronerne: Dette gør bor mere elektronegativt og mindre metallisk end resten af gruppen.
* Højere ioniseringsenergi: Bor kræver mere energi for at fjerne en elektron, hvilket yderligere understøtter dens ikke-metalliske natur.
Derfor, mens bor udviser nogle metalloidegenskaber, er det placeret i gruppe 3A på grund af dets elektroniske konfiguration og lignende kemiske adfærd i visse aspekter. Borons mindre størrelse og unikke egenskaber gør, at den skiller sig ud fra resten af gruppen.
Det er vigtigt at huske, at det periodiske system er et system i konstant udvikling, og placeringen af grundstoffer kan nogle gange være lidt af et kompromis. Borons position afspejler dens fælles elektronkonfiguration og nogle kemiske ligheder med de andre gruppemedlemmer, selvom den udviser forskellige egenskaber.
 Varme artikler
Varme artikler
-
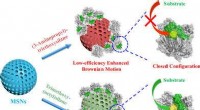 Enzymkonformation påvirker ydeevnen af lipase-drevne nanomotorerKredit:Angewandte Chemie En undersøgelse foretaget af forskere ved Centro Nacional de Investigaciones Cardiovasculares (CNIC), Universidad Complutense (UCM), Universidad de Girona (UdG), og Instit
Enzymkonformation påvirker ydeevnen af lipase-drevne nanomotorerKredit:Angewandte Chemie En undersøgelse foretaget af forskere ved Centro Nacional de Investigaciones Cardiovasculares (CNIC), Universidad Complutense (UCM), Universidad de Girona (UdG), og Instit -
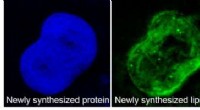 Kortlægning af den indre funktion i en levende celleDa levende celler absorberer tungt vand, deuterium er inkorporeret i nylavede proteiner, lipider og DNA. Da forskerne rettede lyset fra et stimuleret Raman -spredning (SRS) mikroskop mod en enkelt cel
Kortlægning af den indre funktion i en levende celleDa levende celler absorberer tungt vand, deuterium er inkorporeret i nylavede proteiner, lipider og DNA. Da forskerne rettede lyset fra et stimuleret Raman -spredning (SRS) mikroskop mod en enkelt cel -
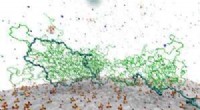 Et hårdt kig på polymerer i cementblandingComputermodeller har afdækket, hvordan superplastikere adsorberes på overfladen af cementpartikler. Kredit:Gengivet fra Ref. 1 og licenseret under CC BY 4.0 2018 T. Hirata et al. Modellering af,
Et hårdt kig på polymerer i cementblandingComputermodeller har afdækket, hvordan superplastikere adsorberes på overfladen af cementpartikler. Kredit:Gengivet fra Ref. 1 og licenseret under CC BY 4.0 2018 T. Hirata et al. Modellering af, -
 AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a
AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a
- Klimaforhandlinger slutter med fremskridt med Paris -regelbogen
- Billig, energieffektiv og ren reaktion til fremstilling af kemisk råmateriale
- Hvad er den type energi, der overføres af langsgående bølger?
- DNA -komplekset med protein kaldes?
- Hvilken dybde fra jordoverfladen er værdiacceleration på grund af tyngdekraften en fjerde på over…
- Hvilke former, når en oceanisk plade tvinges under en anden a. et havbassin b. Ridge c. En subdukti…


