Kovalente bindinger og polaritet:Polariserer alle kovalente molekyler?
Her er hvorfor:
* Polaritet opstår fra ujævn deling af elektroner. Kovalente bindinger opstår, når atomer deler elektroner. Hvis elektronerne deles ligeligt, er bindingen upolær. Hvis et atom trækker de delte elektroner tættere på sig selv, bliver bindingen polær.
* Elektronegativitet bestemmer polariteten. Elektronegativitet er et atoms evne til at tiltrække elektroner. Jo større forskellen er i elektronegativitet mellem to bundne atomer, jo mere polær er bindingen.
* Molekylær geometri spiller også en rolle. Selvom et molekyle har polære bindinger, kan det samlede molekyle være upolært, hvis de polære bindinger er arrangeret symmetrisk, hvilket udligner dipolmomenterne.
Eksempler:
* Ikke-polære kovalente molekyler:
* CO2 (kuldioxid): De to C=O-bindinger er polære, men den lineære form af molekylet betyder, at polariteterne ophæves.
* CH4 (methan): CH-bindingerne er lidt polære, men den tetraedriske form af molekylet gør det upolært.
* Polære kovalente molekyler:
* H2O (vand): O-H-bindingerne er meget polære, og den bøjede form af molekylet betyder, at polariteterne ikke udligner.
* NH3 (ammoniak): N-H-bindingerne er polære, og molekylets pyramideform gør det polært.
Sammenfattende er en kovalent binding et krav for polaritet, men det er ikke den eneste faktor. Elektronegativitetsforskellen mellem atomer og den molekylære geometri bidrager alle til at bestemme, om et molekyle er polært eller upolært.
 Varme artikler
Varme artikler
-
 Forskere opdager en forbindelse mellem to vigtige produkter af nitrogenoxidEksperimenter afslører en hidtil ukendt mekanisme, der ligger til grund for dannelsen af nitrosothioler. Kredit:Daniela Ramos Truzzi Lige siden tre amerikansk-baserede forskere, der arbejder uaf
Forskere opdager en forbindelse mellem to vigtige produkter af nitrogenoxidEksperimenter afslører en hidtil ukendt mekanisme, der ligger til grund for dannelsen af nitrosothioler. Kredit:Daniela Ramos Truzzi Lige siden tre amerikansk-baserede forskere, der arbejder uaf -
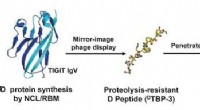 Checkpoint blokade af et D-peptid til cancer immunterapiKredit:Angewandte Chemie Vores immunsystem burde være i stand til at genkende og dræbe tumorceller. Imidlertid, mange tumorer bedrager immunsystemet. For eksempel, de inducerer T-cellers såkaldte
Checkpoint blokade af et D-peptid til cancer immunterapiKredit:Angewandte Chemie Vores immunsystem burde være i stand til at genkende og dræbe tumorceller. Imidlertid, mange tumorer bedrager immunsystemet. For eksempel, de inducerer T-cellers såkaldte -
 Ny indkapslingsteknik beskytter elektroniske egenskaber ved følsomme materialerHZDR-forskere har udviklet en ny metode til at beskytte halvledere fremstillet af følsomme materialer mod kontakt med luft og kemikalier. Det bliver, dermed, muligt at integrere disse ultratynde lag i
Ny indkapslingsteknik beskytter elektroniske egenskaber ved følsomme materialerHZDR-forskere har udviklet en ny metode til at beskytte halvledere fremstillet af følsomme materialer mod kontakt med luft og kemikalier. Det bliver, dermed, muligt at integrere disse ultratynde lag i -
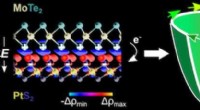 Teori kunne fremskynde skub for spintroniske enhederbilledet til venstre viser krystalstrukturen af et MoTe2|PtS2 heterobillag med isocharge plots fra en model skabt på Rice University. Når materialerne stables sammen, spejlsymmetri er brudt, og der
Teori kunne fremskynde skub for spintroniske enhederbilledet til venstre viser krystalstrukturen af et MoTe2|PtS2 heterobillag med isocharge plots fra en model skabt på Rice University. Når materialerne stables sammen, spejlsymmetri er brudt, og der
- Maskinlæringsteknikker forbedrer røntgenmaterialeanalyse
- Øjeblikkelig hastighed på et øjeblik er lig med størrelsesordenen øjeblikkelig hastighed det ø…
- Hvad en sjælden blodsygdom kan lære os om koagulering
- Hvordan er nåletræer tilpasset deres miljøer?
- Giver energikæder virkelig energi?
- Hvad er dele og funktion af gærcelle?


