Natriums valenselektroner:Forståelse af elektronkonfiguration og reaktivitet
Her er hvorfor:
* Elektronkonfiguration: Natrium har en elektronkonfiguration på 1s² 2s² 2p⁶ 3s¹.
* Yderste skal: Den yderste skal er den 3. skal (n=3).
* Valenselektron: 3s¹ orbitalen indeholder den enkelte valenselektron.
Denne enkeltvalenselektron er det, der gør natrium meget reaktivt og sandsynligvis vil miste det for at danne en positiv ion (Na⁺).
Sidste artikelNatrium- og kloriondannelse:Forståelse af ionisk binding
Næste artikelNatriumion (Na⁺):Forståelse af iondannelse
 Varme artikler
Varme artikler
-
 Ny hybridelektrolyt til højtydende Li-ion-batterierEt fotografi (venstre), henholdsvis et scanningselektronmikroskopbillede (i midten) og en skematisk illustration af sammensat elektrolytstruktur (til højre). Kredit:Grewal og Yabu. Li-ion-batterier
Ny hybridelektrolyt til højtydende Li-ion-batterierEt fotografi (venstre), henholdsvis et scanningselektronmikroskopbillede (i midten) og en skematisk illustration af sammensat elektrolytstruktur (til højre). Kredit:Grewal og Yabu. Li-ion-batterier -
 Team opnår 30 gange forbedring af termoelektrisk ydeevne i polykrystallinsk tinselenidKredit:Tokyo Tech Den fortsatte udtømning af fossile brændstoffer-baserede energiressourcer fører os mod en voksende energikrise. Dette har derfor sat gang i en søgen efter bæredygtige alternative
Team opnår 30 gange forbedring af termoelektrisk ydeevne i polykrystallinsk tinselenidKredit:Tokyo Tech Den fortsatte udtømning af fossile brændstoffer-baserede energiressourcer fører os mod en voksende energikrise. Dette har derfor sat gang i en søgen efter bæredygtige alternative -
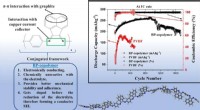 Nyt copolymerbindemiddel for at forlænge levetiden af lithium-ion-batterierNyt copolymerbindemiddel til grafitanode på Li-ion-batterier. BP-copolymeren byder på flere fordele, der sætter den milevidt foran det konventionelle PVDF-bindemiddel med hensyn til stabilitet og hold
Nyt copolymerbindemiddel for at forlænge levetiden af lithium-ion-batterierNyt copolymerbindemiddel til grafitanode på Li-ion-batterier. BP-copolymeren byder på flere fordele, der sætter den milevidt foran det konventionelle PVDF-bindemiddel med hensyn til stabilitet og hold -
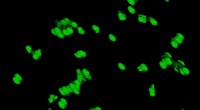 Kostfibre hjælper med at klumpe materiale i din tarmPartikler i tyndtarmsvæsken hos mus ses her i 3D. Musene blev fodret med en standarddiæt. Kredit:Caltech/Ismagilov Lab/A. Preska Steinberg Mad, mikrober, og medicin klumper sig sammen, når de bevæ
Kostfibre hjælper med at klumpe materiale i din tarmPartikler i tyndtarmsvæsken hos mus ses her i 3D. Musene blev fodret med en standarddiæt. Kredit:Caltech/Ismagilov Lab/A. Preska Steinberg Mad, mikrober, og medicin klumper sig sammen, når de bevæ
- Hvidt kattehår på sorte bukser:Undersøgelse måler stabiliteten af præcisionsmasser til gavn f…
- Hvad er nogle interessante fakta om mælkesyre?
- Fysikere får ny indsigt i nanosystemer med sfærisk indeslutning
- Hvad bruges enheden til at måle varmeenergi?
- Hvor mange Apollo -missioner, hvor der til månen?
- Hvilken betydning har stien i forhold til tidevand og sejlads?


