Forståelse af hydrogenioner:kernen af syrer
Her er hvorfor:
* Arrhenius Definition: Denne klassiske definition siger, at en syre er et stof, der producerer hydrogenioner (H+), når det opløses i vand.
* Brønsted-Lowry Definition: Denne bredere definition siger, at en syre er et stof, der donerer en proton (H+).
Eksempler:
* Saltsyre (HCl): Når det opløses i vand, opløses HCl i H+ og Cl-ioner.
* Svovlsyre (H2SO4): Denne stærke syre donerer to protoner og danner 2H+ og SO4^2- ioner.
Vigtig bemærkning: Mens syrer altid har H+ ioner, kan de også have andre ioner afhængigt af den specifikke syre. For eksempel har svovlsyre (H2SO4) også sulfationer (SO4^2-) foruden hydrogenioner.
Sidste artikelSyrer og hydroxylioner:Forstå forskellen
Næste artikelForståelse af hydrogenioner:Nøglen til syreegenskaber
 Varme artikler
Varme artikler
-
 Lad europium skinne klarereEuropium Eu(III)-komplekset med nanocarbon-antenne, der udsender fint rødt lys. Kredit:WPI-ICReDD, Hokkaido Universitet En stablet nanocarbonantenne får et sjældent jordelement til at skinne 5 gan
Lad europium skinne klarereEuropium Eu(III)-komplekset med nanocarbon-antenne, der udsender fint rødt lys. Kredit:WPI-ICReDD, Hokkaido Universitet En stablet nanocarbonantenne får et sjældent jordelement til at skinne 5 gan -
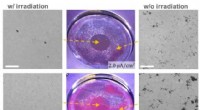 Til ingeniørernes overraskelse, stråling kan bremse korrosion af nogle materialerDisse optiske og scanningselektronmikroskopbilleder viser bestrålede og ubestrålede zoner af en nikkel-chrom legering. Den venstre side viser eksempler på folier med bestråling; i stedet for at forrin
Til ingeniørernes overraskelse, stråling kan bremse korrosion af nogle materialerDisse optiske og scanningselektronmikroskopbilleder viser bestrålede og ubestrålede zoner af en nikkel-chrom legering. Den venstre side viser eksempler på folier med bestråling; i stedet for at forrin -
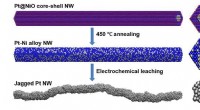 Ru overflader giver yderligere steder for energigenererende reaktioner i brændselscellerFlere aktive steder og mere overfladeareal på katalysatorer fremskynder den kemiske omdannelse af ilt og brint til vand og elektroner, generere elektricitet. Forskere udtænkte en ny synteserute for at
Ru overflader giver yderligere steder for energigenererende reaktioner i brændselscellerFlere aktive steder og mere overfladeareal på katalysatorer fremskynder den kemiske omdannelse af ilt og brint til vand og elektroner, generere elektricitet. Forskere udtænkte en ny synteserute for at -
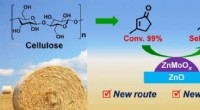 Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake
Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake
- Hvilken type celle kommer ud af mitotisk opdeling?
- Er en formørkelse stopper lyset fra solen ved månen?
- Forståelse af tilstødende atomer og kemiske bindinger:En omfattende vejledning
- Hvordan udøver en elektron en kraft på en anden ladet partikel?
- Ny bog advarer om, at klimaændringer gør os syge
- Små landbrug producerer mere mad end statistik viser


