Støkiometriske koefficienter:Forståelse af kemiske reaktionsformler
Her er en opdeling:
* Stykiometri: Studiet af de kvantitative sammenhænge mellem reaktanter og produkter i kemiske reaktioner.
* Støkiometrisk koefficient: Et tal placeret foran en kemisk formel i en afbalanceret kemisk ligning. Det repræsenterer det relative antal mol af det stof, der er involveret i reaktionen.
Eksempel:
I den afbalancerede kemiske ligning for forbrænding af metan:
CH4 + 2O2 → CO2 + 2H2O
* Den støkiometriske koefficient for metan (CH₄) er 1 .
* Den støkiometriske koefficient for oxygen (O₂) er 2 .
* Den støkiometriske koefficient for kuldioxid (CO₂) er 1 .
* Den støkiometriske koefficient for vand (H₂O) er 2 .
Nøglepunkter om støkiometriske koefficienter:
* De er heltal , ikke brøker.
* De er ikke abonnenter i den kemiske formel.
* De repræsenterer det relative antal mol af hvert stof, der er involveret i reaktionen.
* De bruges til at afbalancere kemiske ligninger , hvilket sikrer, at antallet af atomer i hvert grundstof er det samme på begge sider af ligningen.
Sidste artikelCharles's Lov:Forståelse af forholdet mellem gasvolumen og temperatur
Næste artikelSyrer og hydroxylioner:Forstå forskellen
 Varme artikler
Varme artikler
-
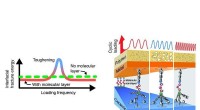 Nanoglue kan gøre kompositter flere gange hårdere under dynamisk belastningIllustrationer af frekvensafhængig hærdning i en polymer-metal-nanogl-keramisk komposit. Kredit:Rensselaer Polytekniske Institut I en opdagelse, der kunne bane vejen for nye materialer og anvendel
Nanoglue kan gøre kompositter flere gange hårdere under dynamisk belastningIllustrationer af frekvensafhængig hærdning i en polymer-metal-nanogl-keramisk komposit. Kredit:Rensselaer Polytekniske Institut I en opdagelse, der kunne bane vejen for nye materialer og anvendel -
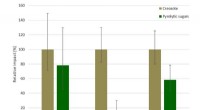 Bæredygtighed af nyt creosotalternativ bekræftetKredit:BTG Biomass Technology Group En nylig offentliggjort undersøgelse har bekræftet bæredygtighedsoplysningerne for et nyt biobaseret alternativ til creosot, der er ved at blive udviklet i Bio4
Bæredygtighed af nyt creosotalternativ bekræftetKredit:BTG Biomass Technology Group En nylig offentliggjort undersøgelse har bekræftet bæredygtighedsoplysningerne for et nyt biobaseret alternativ til creosot, der er ved at blive udviklet i Bio4 -
 Den overraskende videnskab bag hvorfor appelsinskaljuice springer ballonerDen overraskende videnskab bag, hvorfor appelsinskaljuice springer balloner Mange af os husker spændingen ved klasseværelseseksperimenter – ballondrevne biler, natron-vulkaner og den klassiske appels
Den overraskende videnskab bag hvorfor appelsinskaljuice springer ballonerDen overraskende videnskab bag, hvorfor appelsinskaljuice springer balloner Mange af os husker spændingen ved klasseværelseseksperimenter – ballondrevne biler, natron-vulkaner og den klassiske appels -
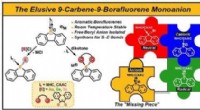 Stabilisering af borafluorenanionen med carbenerKredit:Wiley-VCH, Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202103628 Inkorporeringen af bor i polycykliske aromatiske kulbrintesystemer fører til interessante kromofore
Stabilisering af borafluorenanionen med carbenerKredit:Wiley-VCH, Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202103628 Inkorporeringen af bor i polycykliske aromatiske kulbrintesystemer fører til interessante kromofore
- Fra søvnvaner til kæledyr lærer Amazon-enheder mere. Meget mere
- Rapport viser, at offentlige myndigheder skal tage klimaforandringer alvorligt
- Hvordan påvirker tropiske cykloner luftkvaliteten i Hong Kong?
- Eukaryote organismer:eksempler og karakteristika
- Ældste skrift, der nogensinde er fundet i Israel, identificeret på gammelt keramik
- USAs valgintegritet afhænger af virksomheder, der er udfordret af sikkerheden


