Kogepunktssammenligning:H₂O vs. H₂Se - Forstå forskellen
* Brintbinding: Vand (H2O) molekyler kan danne stærke hydrogenbindinger med hinanden. Disse bindinger skyldes oxygenets høje elektronegativitet, som tiltrækker elektroner væk fra brintatomerne, hvilket skaber en delvis positiv ladning på brinterne og en delvis negativ ladning på oxygenet. Den stærke tiltrækning mellem disse modsatte ladninger resulterer i stærke brintbindinger.
* Svagere intermolekylære kræfter i H₂Se: Hydrogenselenid (H₂Se) har svagere intermolekylære kræfter. Selvom det kan danne dipol-dipol-interaktioner, er disse væsentligt svagere end hydrogenbindinger. Den større størrelse af selen sammenlignet med oxygen betyder, at elektronegativitetsforskellen er mindre, hvilket fører til svagere partielle ladninger og svagere intermolekylære kræfter.
Kogepunktsoversigt:
* Højere kogepunkt: H2O (på grund af stærk hydrogenbinding)
* Lavere kogepunkt: H₂Se (på grund af svagere dipol-dipol-interaktioner)
Sidste artikelFysiske vs. kemiske ændringer:Et historisk perspektiv
Næste artikelAtomer med to uparrede elektroner:En omfattende guide
 Varme artikler
Varme artikler
-
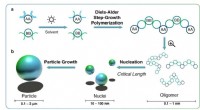 Serendipitous baggårdseksperiment kaster lys over produktion af polymererPrincip for lysinduceret partikeldannelse. a Under bestråling danner en AA-monomer et reaktivt mellemprodukt, som reagerer med en BB-monomer i en Diels-Alder-trinvækstpolymerisation. b Når de lineære
Serendipitous baggårdseksperiment kaster lys over produktion af polymererPrincip for lysinduceret partikeldannelse. a Under bestråling danner en AA-monomer et reaktivt mellemprodukt, som reagerer med en BB-monomer i en Diels-Alder-trinvækstpolymerisation. b Når de lineære -
 Forskere laver biologisk nedbrydelige mikroperler af celluloseDr. Janet Scott, Center for bæredygtige kemiske teknologier, University of Bath. Kredit:University of Bath Forskere og ingeniører fra University of Bath har udviklet bionedbrydelige cellulosemikro
Forskere laver biologisk nedbrydelige mikroperler af celluloseDr. Janet Scott, Center for bæredygtige kemiske teknologier, University of Bath. Kredit:University of Bath Forskere og ingeniører fra University of Bath har udviklet bionedbrydelige cellulosemikro -
 Grafenkrystaller vokser bedre under kobberdækningVækst af enkeltkrystalgrafen ved Cu(111)-Al2O3(0001)-grænsefladen. Kredit:Naturmaterialer (2022). DOI:10.1038/s41563-021-01174-1 En tilgang, der producerer enkeltkrystalgrafenplader på elektrisk is
Grafenkrystaller vokser bedre under kobberdækningVækst af enkeltkrystalgrafen ved Cu(111)-Al2O3(0001)-grænsefladen. Kredit:Naturmaterialer (2022). DOI:10.1038/s41563-021-01174-1 En tilgang, der producerer enkeltkrystalgrafenplader på elektrisk is -
 Ny 3D-røntgenteknik afslører hemmeligheder inde i knoglerneKredit:Tilman Grünewald Et internationalt forskerhold har brugt nye røntgenteknikker til at beskrive, hvordan arkitekturen i sunde menneskelige knogler er bygget op. Holdet har afdækket en hidtil
Ny 3D-røntgenteknik afslører hemmeligheder inde i knoglerneKredit:Tilman Grünewald Et internationalt forskerhold har brugt nye røntgenteknikker til at beskrive, hvordan arkitekturen i sunde menneskelige knogler er bygget op. Holdet har afdækket en hidtil
- Hvad ville du bruge til at simulere en hurtigt flydende lava -vulkan?
- Hvorfor er der ingen skyer på himlen?
- Nano-papir filter fjerner vira
- Er der en opadgående bevægende objekt, der oplever kraft?
- Hvad forbrugere mener, når de siger, at dine produkter er autentiske
- Hvor mange kendte stjerne -konstellationer er der?


