Atomer med to uparrede elektroner:En omfattende guide
Forstå elektronkonfiguration
* Orbitaler: Elektroner optager specifikke energiniveauer kaldet orbitaler. Hver orbital kan maksimalt rumme to elektroner.
* Hunds regel: Når du udfylder orbitaler inden for en subshell (som p-subshell), vil elektroner optage hver orbital individuelt, før de parres.
* Parring: Elektroner i samme orbital vil have modsatte spin.
Find atomer med to uparrede elektroner
1. Identificer elementet: Du skal kende grundstoffets atomnummer for at bestemme dets elektronkonfiguration.
2. Skriv elektronkonfigurationen: Brug det periodiske system og Aufbau-princippet til at skrive elektronkonfigurationen. For eksempel har kulstof (atomnummer 6) konfigurationen 1s² 2s² 2p².
3. Undersøg p-subshell: p-underskallen har tre orbitaler (px, py, pz). Se efter grundstoffer, hvor p-underskallen har to uparrede elektroner.
Eksempler:
* Kulstof (C): 1s² 2s² 2p² - To uparrede elektroner i 2p orbitalerne
* Oxygen (O): 1s² 2s² 2p⁴ - To uparrede elektroner i 2p orbitalerne
* Svovl (S): 1s² 2s² 2p⁶ 3s² 3p⁴ - To uparrede elektroner i 3p-orbitalerne
Vigtig bemærkning: Dette er en forenklet forklaring. Det faktiske antal uparrede elektroner kan blive påvirket af faktorer som hybridisering og elektron-elektron frastødning i mere komplekse atomer.
Sidste artikelKogepunktssammenligning:H₂O vs. H₂Se - Forstå forskellen
Næste artikelNatriumelektronskaller:Forståelse af atomstruktur
 Varme artikler
Varme artikler
-
 Molekylær dans, der kunne eliminere sodforureningReaktiv dimerisering af pi-diradikaler. Kredit:Jacob Martin En skjult, nyopdaget molekylær dans kunne rumme svaret på problemet med sodforurening. Sodforurening forårsager kræft og blodpropper, s
Molekylær dans, der kunne eliminere sodforureningReaktiv dimerisering af pi-diradikaler. Kredit:Jacob Martin En skjult, nyopdaget molekylær dans kunne rumme svaret på problemet med sodforurening. Sodforurening forårsager kræft og blodpropper, s -
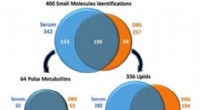 I longitudinelle undersøgelser, tørrede blodpletprøver spiller en rolleVenn -diagrammer illustrerer antallet af serum- og DBS -småmolekyleidentifikationer og overlapningen mellem prøvetyperne. De små molekyler blev adskilt i polære metabolit- og lipididentifikationer og
I longitudinelle undersøgelser, tørrede blodpletprøver spiller en rolleVenn -diagrammer illustrerer antallet af serum- og DBS -småmolekyleidentifikationer og overlapningen mellem prøvetyperne. De små molekyler blev adskilt i polære metabolit- og lipididentifikationer og -
 Natrium er det nye lithium:Forskere finder en måde at øge natriumionbatteriets ydeevne påEn beregning med høj gennemstrømning for Na-migrationsenergier udføres i ca. 4, 300 forbindelser i den uorganiske krystalstrukturdatabase, som forbindelsen faktisk udviste fremragende ydeevne med høj
Natrium er det nye lithium:Forskere finder en måde at øge natriumionbatteriets ydeevne påEn beregning med høj gennemstrømning for Na-migrationsenergier udføres i ca. 4, 300 forbindelser i den uorganiske krystalstrukturdatabase, som forbindelsen faktisk udviste fremragende ydeevne med høj -
 Grænseflade med hjernenNervesystemet er fyldt med kodet information:tanker, følelser, motorstyring. Dette system i vores kroppe er en gåde, og jo mere vi kan gøre for at forstå det, jo mere kan vi gøre for at forbedre menne
Grænseflade med hjernenNervesystemet er fyldt med kodet information:tanker, følelser, motorstyring. Dette system i vores kroppe er en gåde, og jo mere vi kan gøre for at forstå det, jo mere kan vi gøre for at forbedre menne
- Mere end 1, 600 kvadratkilometer brasiliansk Amazonas afskovet i juli
- Hvad er Bacillus megaterium?
- Hvad sker der, når fluor reagerer med vand?
- Hvad er forvitret grundfjeld lavet af?
- Engagerede CO2-udledninger bringer internationale klimamål i fare, undersøgelse finder
- Når lys passerer fra et medium til et andet, hvor det rejser langsommere, er det bøjet normalt?


