Beregning af gasopløselighed ved hjælp af Henrys lov:en trin-for-trin guide
Henrys lov
Henrys lov siger, at opløseligheden af en gas i en væske er direkte proportional med partialtrykket af gassen over væsken. Matematisk:
* S1/P1 =S2/P2
Hvor:
* S1 =Opløselighed ved tryk P1
* S2 =Opløselighed ved tryk P2
Anvendelse af Henrys lov
1. Identificer de kendte:
* S1 =4,0 g/L (opløselighed ved 3,0 ATM)
* P1 =3,0 ATM
* P2 =1,0 ATM
*S2 =? (opløselighed ved 1,0 ATM)
2. Tilslut værdierne i Henrys lovligning:
(4,0 g/L) / (3,0 ATM) =S₂ / (1,0 ATM)
3. Løs for S₂:
S2 =(4,0 g/L * 1,0 ATM) / 3,0 ATM
S₂ =1,33 g/L (ca.)
Svar:
Gassens opløselighed i vand, når trykket over er 1,0 ATM er ca. 1,33 g/L .
Sidste artikelOxidationstal vs. ladning:Forståelse af ioniske forbindelser
Næste artikelKulstof og ilt:Forståelse af atomernes sammensætning
 Varme artikler
Varme artikler
-
 Forskere opdager, at traditionelle væskestrømobservationer kan gå glip af det store billedeEn tidsmæssig reaktion opstod under væskestrømmen indikerede en grundlæggende strukturændring i væskerne. Kredit:Figur tilpasset med tilladelse fra forsiden af J. Phys. Chem. B 2019, 123, 21, 4587-4
Forskere opdager, at traditionelle væskestrømobservationer kan gå glip af det store billedeEn tidsmæssig reaktion opstod under væskestrømmen indikerede en grundlæggende strukturændring i væskerne. Kredit:Figur tilpasset med tilladelse fra forsiden af J. Phys. Chem. B 2019, 123, 21, 4587-4 -
 Forskere lærer mere om de første timer af et lithium-ion-batteris levetidForskere indlæser et specialdesignet lithium-ion-batteri i et sekundært ion-massespektrometer, der giver dem mulighed for at se dannelsen af fast-elektrolyt-interfasen på molekylært niveau, mens bat
Forskere lærer mere om de første timer af et lithium-ion-batteris levetidForskere indlæser et specialdesignet lithium-ion-batteri i et sekundært ion-massespektrometer, der giver dem mulighed for at se dannelsen af fast-elektrolyt-interfasen på molekylært niveau, mens bat -
 Udforsker radiums kemi for at fremme kræftbehandlinger ved hjælp af ioniserende strålingForskere ved Oak Ridge National Laboratory undersøgte radiums kemi for at få nøgleindsigt i at fremme kræftbehandlinger ved hjælp af strålebehandling. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy F
Udforsker radiums kemi for at fremme kræftbehandlinger ved hjælp af ioniserende strålingForskere ved Oak Ridge National Laboratory undersøgte radiums kemi for at få nøgleindsigt i at fremme kræftbehandlinger ved hjælp af strålebehandling. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy F -
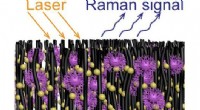 En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i
En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i
- Sådan beregnes diskrete returneringer
- Hvordan kan du finde konstante mængder i fysikvidenskab?
- Hvordan adlyder metaller Lewis Octet -reglen?
- Hvem laver de fineste lab-skabte diamanter?
- En bølge transporterer energi, men betyder ikke noget sandt eller falskt?
- Hvad sker der, når sølvnitrat reagerer med ammoniumchlorid?


