Energi i kemiske reaktioner:input, aktiveringsenergi og varme
Energiinput (reaktanter)
* Aktiveringsenergi: Enhver kemisk reaktion har brug for et indledende "skub" for at starte, kaldet aktiveringsenergi. Denne energi er nødvendig for at bryde bindingerne i reaktanterne og tillade dem at danne nye produkter.
* Varme: Tilførsel af varme giver energi til molekyler, øger deres kinetiske energi og gør dem mere tilbøjelige til at kollidere og reagere.
* Lys: Nogle reaktioner udløses af lysenergi, som fotosyntese.
* Elektrisk energi: Elektrolyse, brugen af elektricitet til at drive en ikke-spontan kemisk reaktion, bruger elektrisk energi som input.
Energioutput (produkter)
* Eksotermiske reaktioner: Disse frigiver energi til omgivelserne, ofte som varme, hvilket gør omgivelserne varmere. Produkterne har lavere energiindhold end reaktanterne.
* Endotermiske reaktioner: Disse absorberer energi fra omgivelserne, hvilket gør omgivelserne koldere. Produkterne har højere energiindhold end reaktanterne.
Nøglebegreber
* Entalpiændring (ΔH): Måler varmeenergiændringen under en reaktion. ΔH er negativ for eksoterme reaktioner (varme frigives) og positiv for endoterme reaktioner (varme absorberes).
* Gibbs Free Energy (ΔG): Forudsiger spontaniteten af en reaktion. En negativ ΔG indikerer en spontan (gunstig) reaktion, mens en positiv ΔG indikerer en ikke-spontan reaktion.
Eksempler:
* Forbrænding: Afbrænding af brændstoffer som træ eller propan er en eksoterm reaktion, der frigiver varme og lys som energiudgange.
* Fotosyntese: Planter bruger lysenergi til at omdanne kuldioxid og vand til glucose og oxygen, en endoterm reaktion.
* Madlavning: Tilberedning af mad involverer endoterme reaktioner, der absorberer varmeenergi fra komfuret for at nedbryde kemiske bindinger og ændre fødevarens sammensætning.
I oversigt
Kemiske reaktioner involverer omdannelse af reaktanter til produkter, og denne proces involverer altid energiændringer. Energitilførslen giver det indledende "skub" for at starte reaktionen, mens energioutputtet kan frigives eller absorberes under processen. At forstå energiinput og -output er afgørende for at forudsige og kontrollere kemiske reaktioner.
Sidste artikelElementer:Forståelse af stoffer med en enkelt type atom
Næste artikelIsotoper og neutroner:Forståelse af atomvariationer
 Varme artikler
Varme artikler
-
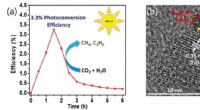 En-to-punch katalysatorer, der fanger kuldioxid til renere brændstofferBrændstofproduktionseffektivitet af titaniumdioxid fotokatalysator med kobber-platin legering co-katalysator (a) og et foto af fotokatalysator observeret af HRTEM (b) Kredit:©DGIST Kobber- og plat
En-to-punch katalysatorer, der fanger kuldioxid til renere brændstofferBrændstofproduktionseffektivitet af titaniumdioxid fotokatalysator med kobber-platin legering co-katalysator (a) og et foto af fotokatalysator observeret af HRTEM (b) Kredit:©DGIST Kobber- og plat -
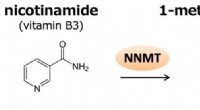 Søjlelignende molekyler som biosensorer for metabolitterNNMT katalyserer methyleringen af nikotinamid til fremstilling af 1-methylnicotinamid (1-MNA). 1-MNA kan yderligere oxideres af aldehydoxidase til, N1-methyl-2-pyridon-5-carboxamid (2py) eller N1-me
Søjlelignende molekyler som biosensorer for metabolitterNNMT katalyserer methyleringen af nikotinamid til fremstilling af 1-methylnicotinamid (1-MNA). 1-MNA kan yderligere oxideres af aldehydoxidase til, N1-methyl-2-pyridon-5-carboxamid (2py) eller N1-me -
 Det rigtige valg af malm kan skabe lavere emissionerTrine Asklund Larssen har undersøgt, hvordan forskellige slags malm i metalproduktion påvirker energiforbrug og udledning. Kredit:Vincent Canaguier, SINTEF I Norge, metalproduktion tegner sig for
Det rigtige valg af malm kan skabe lavere emissionerTrine Asklund Larssen har undersøgt, hvordan forskellige slags malm i metalproduktion påvirker energiforbrug og udledning. Kredit:Vincent Canaguier, SINTEF I Norge, metalproduktion tegner sig for -
 At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af
At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af
- Hvad er forholdet mellem gennemsnitlig kinetisk energi af atomer og temperatur?
- En kraft, der bremser eller stopper et bevægende objekt, er?
- Hvilke objekter indeholder en mekanisme?
- Hvordan dannes et konglomerat rock?
- Nye materialer til fremtidens grønne teknologienheder
- Fe3N2-formel:Forståelse af jern(II)nitrid


