Lithiumreaktivitet:Reaktioner med syrer og baser forklaret
Reaktion med syrer:
* Mekanisme: Lithium er et meget reaktivt alkalimetal. Når den kommer i kontakt med en syre, donerer den let en elektron til de hydrogenioner (H+), der er til stede i syren. Dette resulterer i dannelsen af lithiumioner (Li+) og brintgas (H2).
* Eksempel:
* 2Li(s) + 2HCl(aq) → 2LiCl(aq) + H2(g)
* Reaktionskarakteristika: Disse reaktioner er eksoterme, frigiver varme og producerer en kraftig udvikling af brintgas.
Reaktion med baser:
* Mekanisme: Selvom lithium ikke er så reaktivt med baser, som det er med syrer, kan det stadig reagere. I dette tilfælde reagerer lithium med hydroxidionerne (OH-), der er til stede i basen, og danner lithiumhydroxid (LiOH) og brintgas.
* Eksempel:
* 2Li(s) + 2H2O(l) → 2LiOH(vandig) + H2(g)
* Reaktionskarakteristika: Reaktionen er mindre kraftig end med syrer, men frigiver stadig varme og producerer brintgas.
Vigtige bemærkninger:
* Sikkerhed: Lithiums reaktioner med syrer og baser er meget eksoterme og kan være farlige. Håndter altid lithium forsigtigt og i et godt ventileret område.
* Reaktionsrate: Lithiums reaktivitet med syrer og baser påvirkes af koncentrationen af syren eller basen, temperaturen og overfladearealet af lithium.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
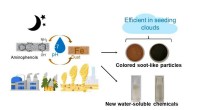 Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf
Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf -
 Skaber mere bæredygtige dufte med bioteknologiKredit:Pixabay/CC0 Public Domain I lyset af et skiftende klima og afgrødesygdomme, Producenter af produkter, der indeholder naturlige smags- og duftstoffer, går over til en ny måde at skaffe ingre
Skaber mere bæredygtige dufte med bioteknologiKredit:Pixabay/CC0 Public Domain I lyset af et skiftende klima og afgrødesygdomme, Producenter af produkter, der indeholder naturlige smags- og duftstoffer, går over til en ny måde at skaffe ingre -
 Uigennemsigtigt plast:definition, nøgletyper og industrielle anvendelserAf Clare Edwards, Opdateret 24. marts 2022 Uigennemsigtig plast er materialer, der blokerer for alt lys, og gør dem fuldstændig ugennemsigtige. Nogle polymerer udviser naturligt denne egenskab på gru
Uigennemsigtigt plast:definition, nøgletyper og industrielle anvendelserAf Clare Edwards, Opdateret 24. marts 2022 Uigennemsigtig plast er materialer, der blokerer for alt lys, og gør dem fuldstændig ugennemsigtige. Nogle polymerer udviser naturligt denne egenskab på gru -
 Højtydende enkeltatomkatalysatorer til høj temperatur brændselscellerKonceptuelt diagram over enkeltatomskatalysator udviklet af KIST -forskere. Kredit:Korea Institue of Science and Technology (KIST) I modsætning til sekundære batterier, der skal genoplades, brænds
Højtydende enkeltatomkatalysatorer til høj temperatur brændselscellerKonceptuelt diagram over enkeltatomskatalysator udviklet af KIST -forskere. Kredit:Korea Institue of Science and Technology (KIST) I modsætning til sekundære batterier, der skal genoplades, brænds
- Hvad er den lyseste stjerne i Big Dipper?
- Konservering og navnløse regnorme:Bedømmere i mørket?
- Origami, 3D-udskrivning smelter sammen for at lave komplekse strukturer i ét skud
- Opstår, når begge halvkugler modtager lige meget sollys?
- Hvem først opdagede viskositet?
- Omfattende model optrævler kvantemekaniske effekter bag fotoluminescens i tynde guldfilm


