Natriumacetat vs. Svovlsyre som katalysatorer:Forståelse af deres roller
* Natriumacetat (CH₃COONa):
* Almindelig brug som basiskatalysator. Det bruges ofte i esterificeringsreaktioner, hvor det hjælper med at neutralisere de sure biprodukter og drive reaktionen fremad.
* Eksempel: Ved esterificering af eddikesyre med ethanol fungerer natriumacetat som en basiskatalysator for at fjerne det producerede vand, hvilket flytter ligevægten mod esterdannelse.
* Svovlsyre (H₂SO4):
* Almindelig brug som en syrekatalysator. Det bruges ofte i dehydreringsreaktioner, hvor det hjælper med at fjerne vandmolekyler fra reaktanter.
* Eksempel: Ved dehydrering af ethanol til dannelse af ethen fungerer svovlsyre som en syrekatalysator til at protonere alkoholen, hvilket gør den mere modtagelig for vandtab.
Valg af den rigtige katalysator afhænger af den specifikke reaktion, du forsøger at udføre.
Nøgleforskelle:
* Surhed: Natriumacetat er en svag base, mens svovlsyre er en stærk syre.
* Reaktionstyper: Natriumacetat bruges ofte i basekatalyserede reaktioner, mens svovlsyre ofte bruges i syrekatalyserede reaktioner.
* Betingelser: Reaktionsbetingelserne (temperatur, koncentration osv.) vil også spille en rolle ved valget af den passende katalysator.
Sammenfattende er der ingen "bedre" katalysator; hver er bedre egnet til forskellige reaktioner baseret på deres specifikke egenskaber.
Sidste artikelBrintgas antændelighed:En simpel demonstration
Næste artikelLithiumreaktivitet:Reaktioner med syrer og baser forklaret
 Varme artikler
Varme artikler
-
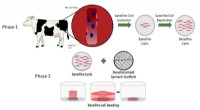 Decellulariseret spinat tjener som en spiselig platform for laboratoriedyrket kødDette diagram viser de trin, Boston College og WPI-forskere tog for at isolere og udså primære bovine satellitceller på et decellulariseret spinatbladstillads. Kredit:Food Bioscience Spinat, et om
Decellulariseret spinat tjener som en spiselig platform for laboratoriedyrket kødDette diagram viser de trin, Boston College og WPI-forskere tog for at isolere og udså primære bovine satellitceller på et decellulariseret spinatbladstillads. Kredit:Food Bioscience Spinat, et om -
 Hydrofob kobberkatalysator for at afbøde elektrolytoversvømmelserDenne hierarkiske kobberstruktur giver CO2-reduktionselektroden tilstrækkelig hydrofobicitet til at bygge en robust gas-væske-fast trefase-grænse. Kredit:NIU Zhuangzhuang et al. Elektroreduktionen
Hydrofob kobberkatalysator for at afbøde elektrolytoversvømmelserDenne hierarkiske kobberstruktur giver CO2-reduktionselektroden tilstrækkelig hydrofobicitet til at bygge en robust gas-væske-fast trefase-grænse. Kredit:NIU Zhuangzhuang et al. Elektroreduktionen -
 Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt
Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt -
 Hvorfor ruster negle? Videnskaben bag jernkorrosionAf Rosann KozlowskiOpdateret 30. august 2022 Den skinnende finish af en frisk negl kan gradvist falme til rødbrune pletter, når den udsættes for elementerne. Den synlige ændring markerer begyndelsen
Hvorfor ruster negle? Videnskaben bag jernkorrosionAf Rosann KozlowskiOpdateret 30. august 2022 Den skinnende finish af en frisk negl kan gradvist falme til rødbrune pletter, når den udsættes for elementerne. Den synlige ændring markerer begyndelsen
- Hvordan 'Shark Week' kunne inspirere til kærlighed til havets rovdyr
- Hvordan er solen som en kæmpe atomreaktor?
- Ternære acceptor- og donormaterialer øger fotonhøst i organiske solceller
- Samsung Electronics nettoresultat falder 52 % i tredje kvartal
- Hvordan en stjernehob udelukkede MACHO'er
- Hvad er vigtigheden af kemi i krige?


