Hvorfor ruster negle? Videnskaben bag jernkorrosion
Af Rosann KozlowskiOpdateret 30. august 2022
Den skinnende finish af en frisk negl kan gradvist falme til rødbrune pletter, når den udsættes for elementerne. Den synlige ændring markerer begyndelsen af rust, en kemisk omdannelse drevet af vand og ilt.
Kemiske årsager til rustdannelse
Korrosion begynder, når vand i miljøet, ofte blandet med kuldioxid, danner en svag syre kaldet kulsyre. Når denne sure opløsning kommer i kontakt med jern, finder to nøglereaktioner sted:
- Det syrnede vand fungerer som en god elektrolyt, der opløser en del af jernet ved at fjerne elektroner.
- Samtidigt nedbrydes vand til brint og oxygen. Den frie ilt reagerer med opløst jern og producerer jernoxid – det vi genkender som rust.
Denne proces kan opsummeres i en simpel ordligning:
Jern + vand + ilt → jernoxid (rust)
Resulterende kemisk reaktion af rust
På molekylært niveau følger rustdannelse efter reaktionen:
4Fe(r) + 3O2 (g) + 6H2 O(l) → 4Fe(OH)3 (s)
Jern(III)hydroxidet, Fe(OH)3 , er porøs og kan yderligere reagere med oxygen for at danne et mere krystallinsk hydrat, Fe2 O3 ·xH2 O. "x"et afspejler, at vandindholdet er variabelt.
Elektrokemisk proces af rust
Rustning opfører sig som et naturligt batteri. Metaloverfladen fungerer som en anode, hvor jernatomer mister elektroner, mens et nærliggende område fungerer som en katode, hvor elektroner forbruges. Vand, som elektrolytten, pendler ioner for at opretholde elektronstrømmen.
Al korrosion er grundlæggende en oxidations-reduktion (redox) reaktion:elektroner forlader metallet og rejser til acceptorer såsom oxygen eller brint.
Rustens to-trins redoxreaktioner
At opdele processen i halvreaktioner tydeliggør elektronbevægelse:
- Oxidation (anode): Fe(r) → Fe 2+ (aq) + 2e -
- Reduktion (katode): O2 (g) + 2H2 O(l) + 4e - → 4OH - (aq)
Når hydroxidioner akkumuleres, kombineres de med jernioner og danner jern(II)hydroxid, som udfælder:
2 Fe 2+ (aq) + 4OH - (aq) → 2Fe(OH)2 (s)
Hvordan rust optræder på et søm
Fordi vand og ilt er allestedsnærværende, vil selv rustfrit stål - en jernrig legering - til sidst ruste, hvis det ikke kontrolleres. Metallets overflade bliver skællende, derefter gruber, og det mere omfangsrige jernoxid udvider sig og forvrænger neglens form. Denne deformation kan få hængsler til at klæbe og knirke. Over tid kan rust nå kernen, hvilket gør metallet skrøbeligt nok til at knække med et enkelt klem.
Selvom salt opløst i vand ikke er en direkte årsag, accelererer det korrosion ved at øge den elektriske ledningsevne.
At forstå disse trin hjælper med at vælge beskyttende belægninger, korrekt opbevaring og vedligeholdelsespraksis for at forlænge levetiden af metalkomponenter.
 Varme artikler
Varme artikler
-
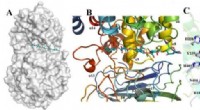 Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce
Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce -
 Styrker lægemiddelopdagelsen ved at evaluere antivirale midler i tusindvis af enkeltcellerEn forbedret mikrofluidisk enhed giver forskere mulighed for samtidig at observere tusindvis af individuelle celler, der er inficeret med virus. Et nærbillede af enheden viser 18 brønde, hver indehold
Styrker lægemiddelopdagelsen ved at evaluere antivirale midler i tusindvis af enkeltcellerEn forbedret mikrofluidisk enhed giver forskere mulighed for samtidig at observere tusindvis af individuelle celler, der er inficeret med virus. Et nærbillede af enheden viser 18 brønde, hver indehold -
 Forskere demonstrerer, hvordan biomolekyleblandinger kommunikerer, interagerer og tilpasser sig dere…Skematisk repræsentation af interaktionslandskab af blandinger af biomolekyler. Kredit:Ella Maru Studio og Ankit Jain En post-doc forsker ved Advanced Science Research Center ved CUNY Graduate Cent
Forskere demonstrerer, hvordan biomolekyleblandinger kommunikerer, interagerer og tilpasser sig dere…Skematisk repræsentation af interaktionslandskab af blandinger af biomolekyler. Kredit:Ella Maru Studio og Ankit Jain En post-doc forsker ved Advanced Science Research Center ved CUNY Graduate Cent -
 Tomater af samme kvalitet som normalt, men bruger kun halvdelen af vandetTomater dyrket med halvdelen af vandet. Kredit:University of Sevilla Eksperter fra University of Sevilla har offentliggjort en undersøgelse, der viser, at en reduktion af vandet, der bruges til
Tomater af samme kvalitet som normalt, men bruger kun halvdelen af vandetTomater dyrket med halvdelen af vandet. Kredit:University of Sevilla Eksperter fra University of Sevilla har offentliggjort en undersøgelse, der viser, at en reduktion af vandet, der bruges til
- Hvad er sammensætningen af lava?
- Vulkanske udbrud dækker ofte skove og bliver til sidst?
- Levende ting består af meget komplicerede molekyler Hvorfor er kulstof vigtig for at danne disse mo…
- Hvad er de faktorer, der påvirker udvælgelse af udstyr?
- Hvorfor bruges pladsprober til at udforske solsystemet?
- Hvad er den ædle gaselektronkonfiguration af strontiumfluorid?


