Forstå AlN:Hvorfor aluminiumnitridformlen bruger denne notation
* Elektronegativitet: Aluminium (Al) er mindre elektronegativt end nitrogen (N). Elektronegativitet er et atoms evne til at tiltrække elektroner i en kemisk binding. Det mindre elektronegative grundstof skrives typisk først i en kemisk formel.
* Kation og anion: Aluminium har tendens til at danne en +3-kation (Al3⁺), mens nitrogen danner en -3-anion (N3⁻). Den positive ion (kation) skrives først i formlen efterfulgt af den negative ion (anion).
* Kemisk binding: Aluminiumnitrid er en ionisk forbindelse. Bindingen dannes af den elektrostatiske tiltrækning mellem de positivt ladede aluminiumioner og de negativt ladede nitrogenioner. Dette forstærker yderligere konventionen om at skrive kationen først.
Derfor er den korrekte formel for aluminiumnitrid AlN, hvilket afspejler grundstoffernes relative elektronegativitet og dannelsen af en kation (Al³⁺) og en anion (N³⁻).
Sidste artikelOxygen til svovl-forhold:Forståelse af kemiske forbindelser
Næste artikelBrintgas antændelighed:En simpel demonstration
 Varme artikler
Varme artikler
-
 På Mars eller Jorden, biohybrid kan omdanne kuldioxid til nye produkterEn enhed til at fange kuldioxid fra luften og omdanne den til nyttige organiske produkter. Til venstre er kammeret indeholdende nanotråd/bakteriehybriden, der reducerer kuldioxid til dannelse af aceta
På Mars eller Jorden, biohybrid kan omdanne kuldioxid til nye produkterEn enhed til at fange kuldioxid fra luften og omdanne den til nyttige organiske produkter. Til venstre er kammeret indeholdende nanotråd/bakteriehybriden, der reducerer kuldioxid til dannelse af aceta -
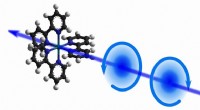 Chiralitet i realtidEn illustration af chiralitet i et molekyle. Kredit:M. Oppermann, EPFL At skelne mellem venstrehåndede og højrehåndede (chirale) molekyler er afgørende i kemi og biovidenskab, og opnås almindeligv
Chiralitet i realtidEn illustration af chiralitet i et molekyle. Kredit:M. Oppermann, EPFL At skelne mellem venstrehåndede og højrehåndede (chirale) molekyler er afgørende i kemi og biovidenskab, og opnås almindeligv -
 Nyudviklet materiale kan føre til lettere, sikrere bildesignKredit:University of Glasgow En ny form for 3-D-printet materiale fremstillet ved at kombinere almindeligt anvendt plast med carbon nanorør er hårdere og lettere end tilsvarende former for alumini
Nyudviklet materiale kan føre til lettere, sikrere bildesignKredit:University of Glasgow En ny form for 3-D-printet materiale fremstillet ved at kombinere almindeligt anvendt plast med carbon nanorør er hårdere og lettere end tilsvarende former for alumini -
 Forskere udvikler computermodel til at forudsige, om et pesticid vil skade bierGrafik viser en AI-tilgang til at bestemme, om et foreslået nyt pesticid er giftigt for honningbier baseret på dets molekylære struktur. Kredit:Cory Simon, Oregon State University Forskere fra Oreg
Forskere udvikler computermodel til at forudsige, om et pesticid vil skade bierGrafik viser en AI-tilgang til at bestemme, om et foreslået nyt pesticid er giftigt for honningbier baseret på dets molekylære struktur. Kredit:Cory Simon, Oregon State University Forskere fra Oreg
- Hvordan påvirker langsomme anomalier under subducerende plader gigantiske megathrust-jordskælv?
- Hvornår landede Neil Armstrong på månen?
- Er alle planeter lyse genstande på himlen?
- Kinas online-servicegigant Meituan sigter mod at rejse 4,4 mia
- At sætte hardwareacceleratorer i gang med automatisk kodeoversættelse
- Hvorfor er det vigtigt at holde et termometer på plads, mens du udfører rektal temperatur?


