Natriumhydroxid- og ammoniumchloridreaktion:Produkter og ligning
1. Ammoniakgas (NH₃): Dette er det mest bemærkelsesværdige produkt. Reaktionen frigiver ammoniakgas, som har en skarp, karakteristisk lugt.
2. Natriumchlorid (NaCl): Dette er et almindeligt salt, der dannes som et biprodukt af reaktionen.
3. Vand (H2O): Vand produceres også under reaktionen.
Den kemiske ligning:
Reaktionen kan repræsenteres ved følgende kemiske ligning:
NaOH(aq) + NH4Cl(aq) → NaCl(aq) + H2O(l) + NH3(g)
Forklaring:
* Natriumhydroxid (NaOH) reagerer med ammoniumchlorid (NH₄Cl) i en syre-base-neutralisering reaktion.
* Hydroxidionerne (OH⁻) fra NaOH reagerer med ammoniumionerne (NH4⁺) fra NH4Cl.
* Denne reaktion frigiver ammoniakgas (NH₃) og danner vand (H₂O).
* De resterende ioner, natrium (Na⁺) og chlorid (Cl⁻), kombineres for at danne natriumchlorid (NaCl).
Observation:
Når du opvarmer blandingen, vil du observere:
* Frigivelse af ammoniakgas, som du kan lugte.
* Dannelse af damp (vanddamp).
* Opløsningen kan blive uklar, når natriumchlorid begynder at fælde ud.
Vigtige bemærkninger:
* Reaktionen er exoterm , hvilket betyder, at den afgiver varme.
* Denne reaktion bruges almindeligvis til at fremstille ammoniakgas i laboratoriet.
* Vær forsigtig, når du håndterer natriumhydroxid, da det er ætsende .
* Udfør altid denne reaktion i et godt ventileret område.
Jeg håber, at denne forklaring hjælper!
 Varme artikler
Varme artikler
-
 Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn: -
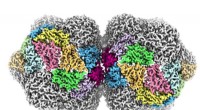 Ødelæggende plantevirus afsløres i atomiske detaljerBilledet viser strukturen af et geminivirus. Kredit:University of Leeds Den komplekse 3D-struktur af en af verdens mest dødelige familier af plantevira er blevet afsløret i enestående detaljer
Ødelæggende plantevirus afsløres i atomiske detaljerBilledet viser strukturen af et geminivirus. Kredit:University of Leeds Den komplekse 3D-struktur af en af verdens mest dødelige familier af plantevira er blevet afsløret i enestående detaljer -
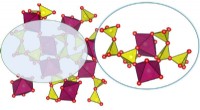 En overlegen, lavpris katalysator til vandspaltningStruktur af NaCo (PO3) 3metaphosphat med et udvidet billede af hjørnedelings [CoO6] octahedra og [PO4] tetraeder byggesten. Kredit:Indian Institute of Science I et væsentligt skridt mod storstilet
En overlegen, lavpris katalysator til vandspaltningStruktur af NaCo (PO3) 3metaphosphat med et udvidet billede af hjørnedelings [CoO6] octahedra og [PO4] tetraeder byggesten. Kredit:Indian Institute of Science I et væsentligt skridt mod storstilet -
 Ny indsigt i overfladeegenskaberne af todimensionelle MXenes-materialerRina Ibragimova. Kredit:Aalto Universitet CEST-forskere har afsløret ny indsigt/resultater om overfladefunktionalisering af materialer, der anvendes i en bred vifte af applikationer, såsom energil
Ny indsigt i overfladeegenskaberne af todimensionelle MXenes-materialerRina Ibragimova. Kredit:Aalto Universitet CEST-forskere har afsløret ny indsigt/resultater om overfladefunktionalisering af materialer, der anvendes i en bred vifte af applikationer, såsom energil
- What represents the highest energy point on an diagram?
- Maskinlæring kan hjælpe os med at forudsige jordskred forårsaget af klimaændringer
- Venstre eller højre? Ny algoritme tager chiralitetsbestemmelse til næste niveau
- Hvad er smeltepunktet i Corten Steel?
- Sofistikerede DNA-laboratorier afsløret for at hjælpe med at spore de savnede
- Skelne mellem en varmeleder og en isolator.?


