Ammoniumchlorid- og natriumhydroxidreaktion:En detaljeret forklaring
NH4Cl(aq) + NaOH(aq) → NaCl(aq) + H2O(l) + NH3(g)
Her er en oversigt over, hvad der sker:
* Ammoniumchlorid (NH4Cl) er et salt, der opløses i vand til dannelse af ammoniumioner (NH4⁺) og chloridioner (Cl⁻).
* Natriumhydroxid (NaOH) er en stærk base, der opløses i vand til dannelse af natriumioner (Na⁺) og hydroxidioner (OH⁻).
Reaktionen:
* Hydroxidioner (OH⁻) fra natriumhydroxid reagerer med ammoniumioner (NH₄⁺) fra ammoniumchloridet.
* Denne reaktion producerer ammoniakgas (NH₃) , som slippes ud i luften.
* Vand (H₂O) er også produceret.
* Natriumchlorid (NaCl) , som er almindeligt bordsalt, forbliver opløst i opløsningen.
Den overordnede reaktion er en syre-base-neutraliseringsreaktion. Ammoniumchlorid virker som en svag syre, mens natriumhydroxid fungerer som en stærk base. Reaktionen producerer et neutralt salt (natriumchlorid) og vand.
Nøgleobservationer:
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og opløsningen bliver varmere.
* En stærk ammoniaklugt vil være til stede på grund af frigivelsen af ammoniakgas.
* Hvis du udfører denne reaktion i et laboratorium, vil du sandsynligvis se, at der dannes bobler, når ammoniakgas slipper ud af opløsningen.
 Varme artikler
Varme artikler
-
 Genbrug og genbrug af slidte katoder til at lave nye lithium-ion-batterierBrugte katodepartikler fra brugte lithium-ion-batterier genbruges og regenereres, så de fungerer så godt som nye. Kredit:David Baillot/UC San Diego Jacobs School of Engineering Nanoingeniører ved
Genbrug og genbrug af slidte katoder til at lave nye lithium-ion-batterierBrugte katodepartikler fra brugte lithium-ion-batterier genbruges og regenereres, så de fungerer så godt som nye. Kredit:David Baillot/UC San Diego Jacobs School of Engineering Nanoingeniører ved -
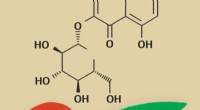 Biokemikere forbinder polyfenoler i ferskenblade med deres ekstrakts antioxidanteffektKredit:RUDN Universitet Biokemikere fra RUDN University har fastslået, hvilke stoffer i ferskenblade, der giver den antioxidante virkning af deres ekstrakt. De undersøgte sammensætningen af pulv
Biokemikere forbinder polyfenoler i ferskenblade med deres ekstrakts antioxidanteffektKredit:RUDN Universitet Biokemikere fra RUDN University har fastslået, hvilke stoffer i ferskenblade, der giver den antioxidante virkning af deres ekstrakt. De undersøgte sammensætningen af pulv -
 Sådan aktiveres molekylsigter:En praktisk vejledning for kemikereAf Jack Brubaker | Opdateret 30. august 2022 Molekylsigter er uundværlige tørremidler i analytisk og syntetisk kemi. Deres åbne-kanal aluminiumsilikatramme fanger vand og andre små molekyler, hvilket
Sådan aktiveres molekylsigter:En praktisk vejledning for kemikereAf Jack Brubaker | Opdateret 30. august 2022 Molekylsigter er uundværlige tørremidler i analytisk og syntetisk kemi. Deres åbne-kanal aluminiumsilikatramme fanger vand og andre små molekyler, hvilket -
 Forskere afslører dynamisk sølvkrystallisering ved in-situ SEMRadikale fluktuationer fører til sølv dynamisk krystallisation i et in-situ scanning elektronmikroskop. Kredit:HAN Yongsheng Forskellige strukturerede materialer har forskellige egenskaber og anve
Forskere afslører dynamisk sølvkrystallisering ved in-situ SEMRadikale fluktuationer fører til sølv dynamisk krystallisation i et in-situ scanning elektronmikroskop. Kredit:HAN Yongsheng Forskellige strukturerede materialer har forskellige egenskaber og anve
- Hvordan får celler den energi, de har brug for, svarer så hurtigt som muligt tak dynger?
- Google hæver annoncegebyrer for at dække østrigsk skat:kilde
- Hvor meget energi frigiver solen?
- Hvordan dannes de resterende bjerge?
- Små røde dyr piler i mørket under isen på en frossen Quebec -sø
- Hvilket mobiltelefonfirma tilbyder de gratis ubegrænsede opkald mellem 2 telefoner?


