Kemiske indikatorer:Hvordan de virker og applikationer
* Farveændring: Dette er den mest almindelige type indikator. Indikatoren skifter farve afhængigt af opløsningens pH. Eksempler omfatter lakmuspapir, phenolphtalein og methylorange.
* Danning af et bundfald: Nogle indikatorer danner et fast bundfald, når de reagerer med målstoffet. Dette kan være nyttigt til at identificere specifikke ioner i opløsning.
* Ændring i fluorescens: Nogle indikatorer udviser fluorescens, som ændrer intensitet eller bølgelængde afhængigt af tilstedeværelsen af analytten.
* Ændring i redoxpotentiale: Nogle indikatorer ændrer farve baseret på analyttens oxidationstilstand.
Her er en oversigt over, hvordan de fungerer:
1. Kemisk reaktion: Indikatormolekylet gennemgår en specifik kemisk reaktion med analytten (det stof, der påvises). Denne reaktion ændrer indikatorens struktur.
2. Ændring af fysisk ejendom: Ændringen i strukturen påvirker direkte en fysisk egenskab ved indikatoren, som derefter kan observeres. Dette kan være en ændring i:
* Farve: Dette sker, når indikatormolekylet absorberer forskellige bølgelængder af lys afhængigt af dets struktur.
* Bundfaldsdannelse: Reaktionen fører til dannelsen af en uopløselig forbindelse, som fremstår som et fast stof i opløsningen.
* Fluorescens: Indikatormolekylets evne til at udsende lys ændres på grund af den strukturelle ændring.
* Redox-potentiale: Indikatorens evne til at acceptere eller donere elektroner ændres, hvilket fører til en farveændring.
3. Visuel observation: Ændringen i indikatorens egenskab giver os mulighed for visuelt at detektere tilstedeværelsen eller fraværet af analytten eller ændringen i den tilstand, der måles.
Eksempler:
* Lakmuspapir: Bliver rød i sure opløsninger og blå i basiske opløsninger.
* Fenolphtalein: Bliver lyserød i basiske opløsninger og er farveløs i sure opløsninger.
* Stivelsesindikator: Danner et dybt blåsort kompleks med jod.
* Kaliumpermanganat: Brugt i redoxtitreringer forsvinder dens lilla farve, efterhånden som den bliver reduceret.
Nøglepunkter at huske:
* Indikatorer bruges typisk i små mængder, og deres tilstedeværelse ændrer ikke væsentligt på den kemiske reaktion, der undersøges.
* Ændringen i indikatoregenskaber er normalt reversibel, hvilket betyder, at indikatoren kan bruges flere gange.
* Valget af indikator afhænger af den specifikke analyt, der detekteres, eller den tilstand, der måles.
Kemiske indikatorer er væsentlige værktøjer inden for forskellige videnskabelige discipliner, herunder kemi, biologi og medicin, til kvalitativ analyse, endepunktsbestemmelse i titreringer og overvågning af forskellige kemiske reaktioner.
Sidste artikelSyre-base neutralisering:definition, proces og reaktion
Næste artikel1-Octanol (C8H17OH):Egenskaber og kemisk formel
 Varme artikler
Varme artikler
-
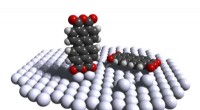 Tricky feat med stand-up molekyleOprejst PTCDA -molekyle på en sølvplatform (til venstre); normalt aflejres molekylet fladt mod det flade lag af sølvatomer (til højre). Kredit:Forschungszentrum Jülich / T. Esat I de seneste årtie
Tricky feat med stand-up molekyleOprejst PTCDA -molekyle på en sølvplatform (til venstre); normalt aflejres molekylet fladt mod det flade lag af sølvatomer (til højre). Kredit:Forschungszentrum Jülich / T. Esat I de seneste årtie -
 Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan
Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan -
 Forskere fremmer indsatsen for nøjagtigt at måle glyphosat-pesticid i havrePrøver af havregryn og havrebaserede produkter analyseret for glyphosat og AMPA. Kredit:J. Murray/NIST Pesticider hjælper landmænd med at øge fødevareproduktionen, reducere dyre skader på afgrøder
Forskere fremmer indsatsen for nøjagtigt at måle glyphosat-pesticid i havrePrøver af havregryn og havrebaserede produkter analyseret for glyphosat og AMPA. Kredit:J. Murray/NIST Pesticider hjælper landmænd med at øge fødevareproduktionen, reducere dyre skader på afgrøder -
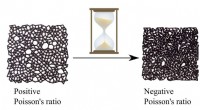 Brug af en materialehukommelse til at kode unikke fysiske egenskaberForskere har vist, at et materiales naturlige ældningsproces kan udnyttes til at skabe materialer med usædvanlige egenskaber. Kredit:Nidhi Pashine En ny undersøgelse offentliggjort i Videnskabens
Brug af en materialehukommelse til at kode unikke fysiske egenskaberForskere har vist, at et materiales naturlige ældningsproces kan udnyttes til at skabe materialer med usædvanlige egenskaber. Kredit:Nidhi Pashine En ny undersøgelse offentliggjort i Videnskabens
- Sådan virker lysforurening
- Hvad driver havbundens spredning? Forståelse af tektonisk pladedynamik
- Hvor meget energi i MW forbruger en lille by med kontorer og indkøbscentre stadioner klubber golfba…
- Prisskilt på planeten? Hjælper virksomhedens værdi med naturen
- Når en kraft forårsager hastigheden af et objekt falder?
- Hvilke forbindelser er reaktanter i processen med cellulær respiration?


