Klor-isotoper:Forståelse af Klor-35 og Klor-37
* Chlor-35 (³⁵Cl): Dette er den mest udbredte isotop, der udgør omkring 75,77% af alle kloratomer. Den har 17 protoner og 18 neutroner i sin kerne.
* Chlor-37 (³⁷Cl): Denne isotop er mindre udbredt og omfatter omkring 24,23% chloratomer. Den har også 17 protoner, men den har 20 neutroner i sin kerne.
Nøgleforskellen mellem disse isotoper er antallet af neutroner:
* Klor-35 har 18 neutroner.
* Klor-37 har 20 neutroner.
Denne forskel i neutrontal resulterer i en lidt højere atommasse for Chlor-37. Begge isotoper har dog det samme antal protoner (17), så de har de samme kemiske egenskaber.
Her er en tabel, der opsummerer de vigtigste forskelle:
| Isotop | Protoner | Neutroner | Atommasse | Overflod (%) |
|---|---|---|---|---|
| Chlor-35 (³⁵Cl) | 17 | 18 | 35,0 u | 75,77 |
| Chlor-37 (37Cl) | 17 | 20 | 37,0 u | 24.23 |
Betydningen af isotoper:
* Gennemsnitlig atommasse: Den gennemsnitlige atommasse af klor (35,45 u) er et vægtet gennemsnit af masserne af dets to isotoper, under hensyntagen til deres relative mængder.
* Kernereaktioner: Isotoper spiller en afgørende rolle i nukleare reaktioner, herunder nuklear fission og fusion.
* Radioaktive isotoper: Nogle isotoper er radioaktive, som klor-36. Disse isotoper bruges i forskellige applikationer, såsom radioaktiv datering og medicinsk billeddannelse.
 Varme artikler
Varme artikler
-
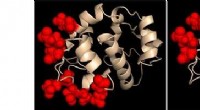 Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst
Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst -
 Tilbereder et ledende alternativ til kobber med aluminiumAluminium er kun en tredjedel af prisen og vægten af kobber, men det er kun omkring 60% som ledende. Aluminiums relativt lave ledningsevne kan være en begrænsning i nogle virkelige applikationer. Kr
Tilbereder et ledende alternativ til kobber med aluminiumAluminium er kun en tredjedel af prisen og vægten af kobber, men det er kun omkring 60% som ledende. Aluminiums relativt lave ledningsevne kan være en begrænsning i nogle virkelige applikationer. Kr -
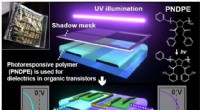 Tuning af fleksible kredsløb med lysFigur 1:Skematisk, der viser processen, der giver mulighed for præcis kontrol af de organiske transistorkarakteristika ved hjælp af lysbestråling. Indsatsen viser et fotografi af den endelige enhed. K
Tuning af fleksible kredsløb med lysFigur 1:Skematisk, der viser processen, der giver mulighed for præcis kontrol af de organiske transistorkarakteristika ved hjælp af lysbestråling. Indsatsen viser et fotografi af den endelige enhed. K -
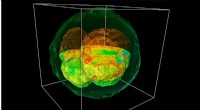 Ny mikroskopteknik afslører indre struktur af levende embryonerEt GLIM billede af et gengivet ko-embryo, der blev skåret gennem midten for at afsløre indre strukturer. Kredit:Billede udlånt af Gabriel Popescu Forskere fra University of Illinois har udviklet e
Ny mikroskopteknik afslører indre struktur af levende embryonerEt GLIM billede af et gengivet ko-embryo, der blev skåret gennem midten for at afsløre indre strukturer. Kredit:Billede udlånt af Gabriel Popescu Forskere fra University of Illinois har udviklet e
- Forskere finder manglende fingerpeg om, hvordan HIV-hackceller udbreder sig
- Satellitkortbrand på Saddleworth Moor
- Hvad er to ressourcer, der kommer fra atmosfæren og beskriver, hvordan begge blev brugt?
- Hvad står G1 for, og hvad sker der i dette trin?
- Hvad sker der med partiklerne af kobbersulfat og jern?
- Hvad er en lille del af rock, der bevæger sig gennem rummet?


