Hvad sker der med partiklerne af kobbersulfat og jern?
reaktionen
Kobbersulfat (cuso₄) er et blåt krystallinsk fast stof, og jern (Fe) er et metallisk element. Når disse to stoffer blandes i en vandig opløsning (vand), en enkelt forskydningsreaktion forekommer.
Her er den kemiske ligning for reaktionen:
cuso₄ (aq) + Fe (s) → feso₄ (aq) + cu (s)
Hvad sker der med partiklerne:
1. jern (Fe) atomer: Jernatomer er mere reaktive end kobberatomer. Når jern introduceres til kobbersulfatopløsningen, mister jernatomerne elektroner (oxidation) og bliver jern (II) -ioner (Fe²⁺) .
2. kobber (II) ioner (Cu²⁺): Kobber (II) ioner i kobbersulfatopløsningen får elektroner (reduktion) og bliver kobberatomer (Cu) .
3. sulfationer (so₄²⁻): Sulfationer forbliver uændrede under hele reaktionen. De er tilskuerioner, hvilket betyder, at de er til stede i løsningen, men deltager ikke direkte i den kemiske ændring.
Resultatet
* jernsulfat (feso₄) Formularer i opløsningen. Jernsulfat er normalt en grønblå farve.
* kobber (cu) deponeres som et rødbrunt fast stof. Du vil se dette som en belægning eller sediment, der dannes i reaktionsbeholderen.
Partikelniveau Forklaring:
* På atomniveau donerer jernatomer elektroner til kobber (II) -ioner.
* Denne elektronoverførsel får jernatomerne til at blive positivt ladede ioner (Fe²⁺) og kobber (II) ioner til at blive neutrale kobberatomer (Cu).
Nøglepunkter
* Reaktionen er en enkelt forskydningsreaktion, hvor et mere reaktivt metal (jern) fortrænger et mindre reaktivt metal (kobber) fra dens saltopløsning.
* Reaktionen involverer overførsel af elektroner (oxidationsreduktion), hvilket fører til dannelse af nye forbindelser.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvad er hastigheden af kemisk vejrforhold øges med dette?
Næste artikelHvilken er mere reaktiv zink eller nikkel?
 Varme artikler
Varme artikler
-
 Svejsning med stamceller til næste generations kirurgiske limKredit:CC0 Public Domain Forskere ved University of Bristol har opfundet en ny teknologi, der kan føre til udviklingen af en ny generation af smarte kirurgiske lim og forbindinger til kroniske s
Svejsning med stamceller til næste generations kirurgiske limKredit:CC0 Public Domain Forskere ved University of Bristol har opfundet en ny teknologi, der kan føre til udviklingen af en ny generation af smarte kirurgiske lim og forbindinger til kroniske s -
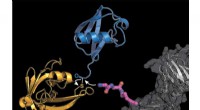 Mærkning af proteiner med ubiquitin baner ny vej til forskning i cellereguleringForskerne udstyrede et cellulært protein (gråt) med en modificeret lysinaminosyre byggesten (lyserød), hvortil det bakterielle enzym sortase (gul) transmitterer et ubiquitinmolekyle (blåt). Kredit:K.
Mærkning af proteiner med ubiquitin baner ny vej til forskning i cellereguleringForskerne udstyrede et cellulært protein (gråt) med en modificeret lysinaminosyre byggesten (lyserød), hvortil det bakterielle enzym sortase (gul) transmitterer et ubiquitinmolekyle (blåt). Kredit:K. -
 DNA som en supramolekylær byggestenKredit:Leiden Universitet Ph.d.-studerende Willem Noteborn har undersøgt supramolekylære strukturer. Disse kan være nyttige til indlæsning af medicin og signalmolekyler vedr. for eksempel, cellulæ
DNA som en supramolekylær byggestenKredit:Leiden Universitet Ph.d.-studerende Willem Noteborn har undersøgt supramolekylære strukturer. Disse kan være nyttige til indlæsning af medicin og signalmolekyler vedr. for eksempel, cellulæ -
 Hvordan computere søger efter fremtidens stofferKredit:University of California, San Francisco Opdagelse af lægemidler kan bringe tankerne hen på billeder af hvide laboratoriefrakker og pipetter, men da Henry Lin, PhD, for nylig satte sig for a
Hvordan computere søger efter fremtidens stofferKredit:University of California, San Francisco Opdagelse af lægemidler kan bringe tankerne hen på billeder af hvide laboratoriefrakker og pipetter, men da Henry Lin, PhD, for nylig satte sig for a
- Hvorfor er elektricitet en form for energi?
- Hvordan reproducerer fladorm og rundorm?
- Hvordan hirse opretholdt Mongoliets imperier
- Hvordan produceres smedejern?
- Foxconn siger, at der ikke er planlagt ændringer for Wisconsin-projektet
- Hvordan ville du forklare acceleration til ven eller slægtning inklusive enheder?


