Kovalente bindinger:Forståelse af reglen om elektronegativitetsforskel
0,4-elektronegativitetsforskelreglen:
* Sandt: En forskel i elektronegativitet under 0,4 er mere tilbøjelig til at resultere i en ikke-polær kovalent binding . I ikke-polære kovalente bindinger deles elektroner ligeligt mellem atomerne.
* Ikke altid nøjagtige: Elektronegativitetsforskellen alene bestemmer ikke altid typen af binding. Andre faktorer som:
* De specifikke involverede atomer: Selv med en lille forskel kan tilstedeværelsen af meget elektronegative atomer som oxygen eller fluor stadig resultere i en let polær binding.
* Den overordnede molekylære geometri: Selv med ikke-polære bindinger kan formen af molekylet skabe et dipolmoment, hvilket gør det polært generelt.
Vigtige overvejelser:
* Polære kovalente bindinger: Elektronegativitetsforskelle mellem 0,4 og 1,7 resulterer generelt i polære kovalente bindinger . Elektroner deles ikke ligeligt, hvilket fører til delvise positive og negative ladninger på atomerne.
* ioniske bindinger: Elektronegativitetsforskelle større end 1,7 fører normalt til ioniske bindinger . Elektroner overføres fra et atom til et andet, hvilket resulterer i ladede ioner, der holdes sammen af elektrostatiske kræfter.
Opsummering:
Selvom 0,4-reglen er en nyttig retningslinje, er det afgørende at huske, at andre faktorer bidrager til den type binding, der dannes. Det er bedst at bruge elektronegativitet som et af flere værktøjer til at analysere bindingskarakteristika.
 Varme artikler
Varme artikler
-
 Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und
Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und -
 Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte
Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte -
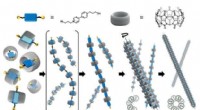 Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t
Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t -
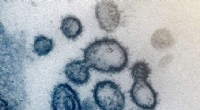 COVID-19 sætter ny videnskab til presstestenDette transmissionselektronmikroskopbillede viser SARS-CoV-2-også kendt som 2019-nCoV, virussen, der forårsager COVID-19-isoleret fra en patient i USA. Viruspartikler vises fra overfladen af celler
COVID-19 sætter ny videnskab til presstestenDette transmissionselektronmikroskopbillede viser SARS-CoV-2-også kendt som 2019-nCoV, virussen, der forårsager COVID-19-isoleret fra en patient i USA. Viruspartikler vises fra overfladen af celler


