Hvor mange nanopartikler opvarmer tumoren?
De, der skal bekæmpe en stærk fjende, skal lede efter allierede. Det er grunden til, at fysikere fra forskellige videnskabelige områder har besluttet at samarbejde med biomedicinske læger for at placere kampen mod kræft gennem varmebehandling ved hjælp af magnetiske nanopartikler på et fast stof, videnskabeligt grundlag. Det er formålet med samarbejdet at forbedre terapiens succes. Inden for rammerne af et fælles projekt finansieret af Deutsche Forschungsgemeinschaft, Melanie Kettering fra Institut für Diagnostische und Interventionelle Radiologie (IDIR), Universitetshospitalet Jena, og Heike Richter fra Physikalisch-Technische Bundesanstalt (PTB) er ansvarlige for opgaven med at opdage, hvor mange magnetiske nanopartikler kan findes i patientens krop.
De sprøjtes ind i tumoren - men bliver de virkelig der, eller er de fordelt i hele kroppen? At vide, hvor mange der er i tumoren, er vigtigt for varmebehandlingens succes. Nu er det lykkedes forskerne at påvise på mus, at magnetisk relaxometri er velegnet til at blive anvendt sammen med varmebehandlingen. Den giver information om, hvor nanopartiklerne befinder sig i kroppen - helt uden kontakt til patienten.
Til kræftbehandling ved hjælp af varmebehandling, magnetiske nanopartikler sprøjtes ind i tumoren og exciteres af en ekstern elektromagnetisk a.c. Mark. Igennem dette, de magnetiske nanopartikler genererer varme inde i tumoren. Hvis temperaturer mellem 55 °C og 60 °C nås, kræftceller kan ødelægges irreversibelt. Det omgivende sunde væv (uden magnetiske nanopartikler) forbliver upåvirket. Proceduren har endnu ikke fundet vej til den kliniske rutine, men er stadig i prøvefasen, da en række spørgsmål stadig mangler at blive afklaret. Blandt andet, Der kræves en procedure, som viser, hvor nanopartiklerne befinder sig i kroppen, og i hvilken mængde de kan findes der. På dette grundlag, en selektiv behandling af tumoren kan opnås. PTB-forskere har fundet ud af, at magnetisk relaxometri er meget velegnet til at indhente denne information - uden selv at røre ved patientens krop eller på anden måde skade hende/ham.
Dette gøres på følgende måde, inden behandlingen som sådan påbegyndes:Jernoxid-nanopartiklerne, der sprøjtes ind i tumoren, er superparamagnetiske, dvs. de er små magnetiske partikler, som kan ændre deres magnetiseringsretning uafhængigt af hinanden. Ved stuetemperatur, deres orientering i rummet er statistisk fordelt, så deres sum ikke danner et magnetisk moment. Hvis et eksternt konstant magnetfelt nu påføres, de orienterer sig alle næsten identisk i rummet langs feltet og genererer et magnetisk moment, som kan måles udefra. Dette magnetfelt slukkes derefter og med følsomme magnetfeltsensorer, såkaldte SQUID'er (Superconducting Quantum Interference Devices, superledende kvanteinterferensenheder), den følgende relaksering af magnetiseringen - dvs. tilbagevenden af det magnetiske moment fra den ensartede orientering til en tilstand med en statistisk fordeling - bestemmes ekstremt hurtigt. Amplituden af relaksationssignalet giver så information om partikelmængden.
De hidtidige undersøgelser på mus gør det muligt at drage den konklusion, at injektionen af magnetiske nanopartikler og partiklernes opholdssted på injektionsstedet fungerer varierende godt. I nogle tumorer, forskerne kunne finde - 24 timer efter injektionen - den næsten fuldstændige mængde af nanopartikler i kræften, hvorimod i andre tumorer kun en fjerdedel af de injicerede partikler kunne påvises. Indtil nu, det har ikke været muligt at finde en velbegrundet forklaring på disse forskellige mængder af magnetiske nanopartikler i tumoren. Imidlertid, Resultatet viser så meget desto mere, hvor vigtigt det er at anvende magnetisk relaxometri samtidig med varmebehandlingen af kræft med nanopartikler for at kunne udtale sig om mængden af partikler i tumoren. (ptb/hvis)
 Varme artikler
Varme artikler
-
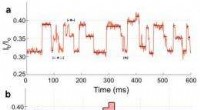 Lille læser gør hurtigt, billig DNA -sekventering muligDe forskellige niveauer af elektrisk signal fra sekvensen af en DNA -streng trukket gennem en nanopore -læser (øverst) svarer til specifikke DNA -nukleotider, thymin, adenin, cytosin og guanin (nede
Lille læser gør hurtigt, billig DNA -sekventering muligDe forskellige niveauer af elektrisk signal fra sekvensen af en DNA -streng trukket gennem en nanopore -læser (øverst) svarer til specifikke DNA -nukleotider, thymin, adenin, cytosin og guanin (nede -
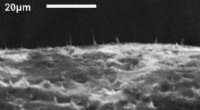 Forskere skaber fleksible, nanoskala af negle til mulig lægemiddeltilførselDette billede viser carbon nanofiber nåle indlejret i en elastisk silikone membran. Kredit:Anatoli Melechko, North Carolina State University Forskere ved North Carolina State University har fundet
Forskere skaber fleksible, nanoskala af negle til mulig lægemiddeltilførselDette billede viser carbon nanofiber nåle indlejret i en elastisk silikone membran. Kredit:Anatoli Melechko, North Carolina State University Forskere ved North Carolina State University har fundet -
 Brug af guldpartikler til at bekæmpe kræftForskere ved MIRA Institute for Biomedical Technology and Technical Medicine, University of Twente, Holland, udvikler en metode til at opdage og behandle tumorer ved hjælp af guldpartikler med dimensi
Brug af guldpartikler til at bekæmpe kræftForskere ved MIRA Institute for Biomedical Technology and Technical Medicine, University of Twente, Holland, udvikler en metode til at opdage og behandle tumorer ved hjælp af guldpartikler med dimensi -
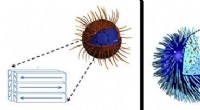 Nanopartikler til at dræbe kræftceller med varmeJernoxidnanopartikler med en pænt stablet indre struktur (venstre) har brug for et stærkere magnetfelt end forventet for at varme op, mens dem med et mere tilfældigt arrangement opvarmes hurtigere, se
Nanopartikler til at dræbe kræftceller med varmeJernoxidnanopartikler med en pænt stablet indre struktur (venstre) har brug for et stærkere magnetfelt end forventet for at varme op, mens dem med et mere tilfældigt arrangement opvarmes hurtigere, se
- Hvilken type dyr spiser planter?
- Laserfordampningsteknologi til at skabe nye solmaterialer
- Tyfoner og andre katastrofer tvinger Japan til at gentænke sin by mod landdistrikterne for fremtide…
- Hvordan beregner jeg gentagelighed?
- Et mindretal af lande tilbyder gratis førskoleundervisning, rapporterer forskere
- Den ekstraordinære oprindelse af EUV -lys i varmt tinplasma


