Kovalente vs. ioniske bindinger:En omfattende vejledning
Kovalente bindinger og ioniske bindinger:
Kovalente bindinger:
* Formation: Dannes, når to atomer deles elektroner for at opnå en stabil elektronkonfiguration.
* Natur: Ikke-metalatomer med lignende elektronegativitet deler elektroner og danner en stærk binding.
* Egenskaber:
* Opstår normalt mellem to ikke-metalatomer.
* Høje smelte- og kogepunkter.
* Dårlige ledere af elektricitet.
* Kan være polær eller ikke-polær.
* Eksempler: Vand (H₂O), Kuldioxid (CO₂), Methan (CH₄)
Ioniske bindinger:
* Formation: Dannes, når ét atom overføres en elektron til et andet atom, hvilket skaber modsat ladede ioner, som så tiltrækkes af hinanden.
* Natur: Opstår mellem et metalatom (tendens til at tabe elektroner) og et ikke-metalatom (tendens til at få elektroner).
* Egenskaber:
* Opstår normalt mellem et metal og et ikke-metal.
* Høje smelte- og kogepunkter.
* Gode ledere af elektricitet, når de er opløst i vand eller smeltet.
* Danner typisk krystallinske faste stoffer.
* Eksempler: Natriumchlorid (NaCl), Calciumoxid (CaO), Magnesiumfluorid (MgF₂)
Her er en tabel, der opsummerer de vigtigste forskelle:
| Funktion | Kovalent binding | Ionisk binding |
|--------------------|--------------------------------|----------------------------------------------------|
| Formation | Deling af elektroner | Overførsel af elektroner |
| Involverede atomer | Normalt to ikke-metaller | Metal og ikke-metal |
| Elektronegativitet | Lignende elektronegativitet | Meget forskellig elektronegativitet |
| Smelte-/kogepunkt | Generelt høj | Høj |
| Konduktivitet | Dårlig, undtagen grafit | God, når den er opløst eller smeltet |
| Struktur | Molekyler | Krystallinske faste stoffer |
| Eksempler | Vand, metan, kuldioxid | Natriumchlorid, calciumoxid, magnesiumfluorid |
Som konklusion: Både kovalente og ioniske bindinger er afgørende for at skabe stabile molekyler og forbindelser, men de adskiller sig i deres dannelse, egenskaber og de involverede typer atomer. At forstå disse forskelle er afgørende for at forstå karakteren af kemisk binding.
 Varme artikler
Varme artikler
-
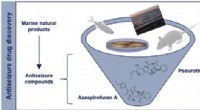 Svamp i Rødehavet giver spor til nye epilepsimedicinKredit:American Chemical Society Nye behandlinger for epilepsi er hårdt nødvendige, fordi den nuværende medicin ikke virker for mange mennesker med sygdommen. For at finde nye kundeemner, forskere
Svamp i Rødehavet giver spor til nye epilepsimedicinKredit:American Chemical Society Nye behandlinger for epilepsi er hårdt nødvendige, fordi den nuværende medicin ikke virker for mange mennesker med sygdommen. For at finde nye kundeemner, forskere -
 Opfinder verdens stærkeste sølvInde i et sølvkorn, kobberatomurenheder (i grønt) er blevet selektivt adskilt til en korngrænse (til venstre) og til indre defekter (lange strenge, streamer nedad.) Dette øjebliksbillede, fra en atomi
Opfinder verdens stærkeste sølvInde i et sølvkorn, kobberatomurenheder (i grønt) er blevet selektivt adskilt til en korngrænse (til venstre) og til indre defekter (lange strenge, streamer nedad.) Dette øjebliksbillede, fra en atomi -
 Forskere udvikler materialer, der kan revolutionere, hvordan lys udnyttes til solenergiMagnetfeltdata, der viser dannelsen og forfaldet af excitonerne genereret af singlet fission. Kredit:A. Asadpoor Darvish, McCamey Lab Forskere ved Columbia University har udviklet en måde at udn
Forskere udvikler materialer, der kan revolutionere, hvordan lys udnyttes til solenergiMagnetfeltdata, der viser dannelsen og forfaldet af excitonerne genereret af singlet fission. Kredit:A. Asadpoor Darvish, McCamey Lab Forskere ved Columbia University har udviklet en måde at udn -
 Metal-organiske rammer kan adskille gasser på trods af tilstedeværelsen af vandEn visualisering af strukturen af metal-organiske rammer med metallet (kobolt, blå) i hjørnerne og de organiske strukturer, der spænder over siderne (kulstof, grå; ilt, rød). Kredit:Vervoorts P. et
Metal-organiske rammer kan adskille gasser på trods af tilstedeværelsen af vandEn visualisering af strukturen af metal-organiske rammer med metallet (kobolt, blå) i hjørnerne og de organiske strukturer, der spænder over siderne (kulstof, grå; ilt, rød). Kredit:Vervoorts P. et


