Iltelektronkonfiguration:Forståelse af 1s² 2s² 2p⁴
1s² 2s² 2p⁴
Sådan forstår du det:
* 1s²: Det første energiniveau (n=1) har én underskal, s-underskallen, som kan rumme op til 2 elektroner. Ilt har 2 elektroner i denne underskal.
* 2s²: Det andet energiniveau (n=2) har også en s underskal, som igen rummer 2 elektroner. Ilt har 2 elektroner i denne underskal.
* 2p⁴: Det andet energiniveau har også en p-underskal, som kan rumme op til 6 elektroner. Ilt har 4 elektroner i denne underskal.
Sig til, hvis du gerne vil se en mere visuel repræsentation af dette!
Sidste artikelKulstofatomer i et mol butan:En detaljeret beregning
Næste artikelFysisk forandring:Is til vand forklaret - kemibegreber
 Varme artikler
Varme artikler
-
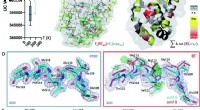 Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde
Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde -
 Brændselscellekatalysatorers aktivitet blev fordobletDet er lykkedes et tværfagligt forskerteam ved det tekniske universitet i München (TUM) at optimere størrelsen af platin -nanopartikler til brændselscellekatalyse, så de nye katalysatorer er dobbelt
Brændselscellekatalysatorers aktivitet blev fordobletDet er lykkedes et tværfagligt forskerteam ved det tekniske universitet i München (TUM) at optimere størrelsen af platin -nanopartikler til brændselscellekatalyse, så de nye katalysatorer er dobbelt -
 Undersøgelse af opvarmede tobaksprodukterKredit:Pixabay/CC0 Public Domain En ny artikel, der undersøger, om opvarmede tobaksprodukter udsender røg, er blevet offentliggjort i det akademiske tidsskrift American Chemical Society Omega . Pr
Undersøgelse af opvarmede tobaksprodukterKredit:Pixabay/CC0 Public Domain En ny artikel, der undersøger, om opvarmede tobaksprodukter udsender røg, er blevet offentliggjort i det akademiske tidsskrift American Chemical Society Omega . Pr -
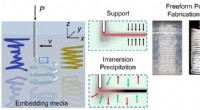 Unik metode til at fremstille friformede strukturer af termoplast i mikropartikelformige gelerEn polymerblæk udskrives af en DIW 3D-printer i Bingham-plastikmikropartikelgeler som indlejringsmedie. De omgivende indlejringsmedier understøttede de trykte blæk og forårsagede in situ faseadskillel
Unik metode til at fremstille friformede strukturer af termoplast i mikropartikelformige gelerEn polymerblæk udskrives af en DIW 3D-printer i Bingham-plastikmikropartikelgeler som indlejringsmedie. De omgivende indlejringsmedier understøttede de trykte blæk og forårsagede in situ faseadskillel


