Flygtighedssammenligning:ioniske vs. kovalente forbindelser - en videnskabelig forklaring
Volatilitet refererer til et stofs tendens til at fordampe eller fordampe ved en given temperatur.
Ioniske forbindelser holdes sammen af stærke elektrostatiske kræfter mellem modsat ladede ioner. Disse kræfter er meget stærke og kræver en betydelig mængde energi at overvinde, hvilket resulterer i:
* Høje smelte- og kogepunkter: Ionforbindelser har høje smelte- og kogepunkter, fordi der skal meget energi til for at bryde de stærke ionbindinger.
* Lav volatilitet: På grund af de stærke interioniske kræfter har ioniske forbindelser lav flygtighed. De har tendens til at forblive i fast tilstand ved stuetemperatur og fordamper ikke let.
Kovalente forbindelser holdes sammen af svagere kovalente bindinger, som involverer deling af elektroner mellem atomer. Disse bindinger er generelt svagere end ioniske bindinger, hvilket fører til:
* Lavere smelte- og kogepunkter: Kovalente forbindelser har lavere smelte- og kogepunkter sammenlignet med ioniske forbindelser.
* Højere volatilitet: De svagere bindinger i kovalente forbindelser tillader dem at fordampe lettere. Dette resulterer i en højere volatilitet.
Eksempler:
* Ionisk forbindelse: Natriumchlorid (NaCl) har et højt smeltepunkt (801 °C) og er ikke-flygtigt ved stuetemperatur.
* Kovalent forbindelse: Vand (H2O) har et relativt lavt kogepunkt (100 °C) og er relativt flygtigt.
Undtagelser:
Der er nogle undtagelser fra denne generelle regel. For eksempel kan nogle ioniske forbindelser, såsom kviksølv(I)chlorid (Hg2Cl2), være flygtige ved forhøjede temperaturer.
Opsummering:
Ioniske forbindelser har generelt lav flygtighed på grund af de stærke elektrostatiske kræfter, der holder dem sammen. Kovalente forbindelser har typisk højere flygtighed på grund af de svagere kovalente bindinger mellem atomer.
 Varme artikler
Varme artikler
-
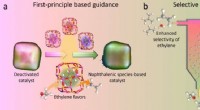 Forskere regenererer deaktiveret katalysator i methanol-til-olefin-processena. Første-principbaserede simuleringer giver kriterierne for stabilitet og funktionalitet af organiske mellemprodukter indespærret i nano-hulrum. b Selektiv omdannelse af koks til en specifik naphthal
Forskere regenererer deaktiveret katalysator i methanol-til-olefin-processena. Første-principbaserede simuleringer giver kriterierne for stabilitet og funktionalitet af organiske mellemprodukter indespærret i nano-hulrum. b Selektiv omdannelse af koks til en specifik naphthal -
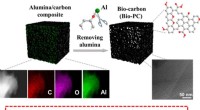 Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re
Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re -
 Kviksølvfjernelse gjort let i giftige miljøerKredit:Pixabay/CC0 Public Domain Kviksølvforurening er et globalt problem i vand, luft og jord i nærheden af guldminer, cement og noget metalproduktion og andre tunge industrier, der brænder foss
Kviksølvfjernelse gjort let i giftige miljøerKredit:Pixabay/CC0 Public Domain Kviksølvforurening er et globalt problem i vand, luft og jord i nærheden af guldminer, cement og noget metalproduktion og andre tunge industrier, der brænder foss -
 Sikring af broccolispirer bevarer deres kræftbekæmpende forbindelserKredit:CC0 Public Domain Rå broccolispirer, en rig kilde til potentielle kræftbekæmpende forbindelser, er blevet en populær helsekost i de seneste år. Men konventionel varmebehandling, der bruges
Sikring af broccolispirer bevarer deres kræftbekæmpende forbindelserKredit:CC0 Public Domain Rå broccolispirer, en rig kilde til potentielle kræftbekæmpende forbindelser, er blevet en populær helsekost i de seneste år. Men konventionel varmebehandling, der bruges
- Hvad er breddegrad (grader) til Orion?
- Sådan certificeres en kvantecomputer
- Hvilken teori siger, at månen dannede sig, da et objekt i planetstørrelse kolliderede med Jorden?
- Hvor meget nano3 opløses i 100 g vand en 30 ° C?
- Hvad hedder en sedimentær klippe normalt baseret på?
- Biobaserede drikkekartoner


