Kationer:Forståelse af 2+ ladede ioner og deres eksempler
Gruppe 2-elementer (jordalkalimetaller)
* Calcium (Ca²⁺) - Findes i knogler, tænder og spiller en rolle i muskelsammentrækning.
* Magnesium (Mg²⁺) - Findes i klorofyl, afgørende for fotosyntesen.
* Barium (Ba²⁺) - Bruges i fyrværkeri til grøn farve.
* Strontium (Sr²⁺) - Bruges i fyrværkeri til rød farve.
Overgangsmetaller
* Jern (Fe²⁺) - Til stede i hæmoglobin, ansvarlig for ilttransport.
* Kobber (Cu²⁺) - Anvendes i elektriske ledninger og VVS.
* Zink (Zn²⁺) - Vigtig for immunfunktion og sårheling.
* Mangan (Mn²⁺) - Involveret i stofskifte og knogledannelse.
Andre eksempler
* Bly (Pb²⁺) - Et giftigt tungmetal.
* Kviksølv (Hg²⁺) - Et giftigt tungmetal.
* Nikkel (Ni²⁺) - Anvendes i batterier og legeringer.
* Kobolt (Co²⁺) - Findes i vitamin B12.
Sådan bestemmes ladningen af en ion:
* Gruppe 1-elementer (alkalimetaller): +1 opladning
* Gruppe 2-elementer (jordalkalimetaller): +2 opladning
* Halogener (Gruppe 17): -1 opladning
* Oxygen (Gruppe 16): -2 opladninger
* Overgangsmetaller: Varierende ladninger, ofte bestemt af den forbindelse, de danner.
Det er vigtigt at bemærke, at ladningen af en ion kan bestemmes af dens position på det periodiske system og dens elektronkonfiguration.
 Varme artikler
Varme artikler
-
 Forskere producerer biobrændstof til konventionelle dieselmotorerLukas Gooßen i sit laboratorium i Bochum. Kredit:RUB, Kramer I overensstemmelse med et EU -direktiv, konventionel bildiesel suppleres med 7 procent biodiesel. Denne andel forventes at stige til ti
Forskere producerer biobrændstof til konventionelle dieselmotorerLukas Gooßen i sit laboratorium i Bochum. Kredit:RUB, Kramer I overensstemmelse med et EU -direktiv, konventionel bildiesel suppleres med 7 procent biodiesel. Denne andel forventes at stige til ti -
 Filmteknologi inspirerer til bærbar flydende enhed, der har til formål at høste energiEt team fra Purdue University skabte bærbar teknologi til at omdanne mekanisk energi til elektrisk energi. Kredit:Wenzhuo Wu/Purdue University En fascination af filmteknologi, der viste, at robott
Filmteknologi inspirerer til bærbar flydende enhed, der har til formål at høste energiEt team fra Purdue University skabte bærbar teknologi til at omdanne mekanisk energi til elektrisk energi. Kredit:Wenzhuo Wu/Purdue University En fascination af filmteknologi, der viste, at robott -
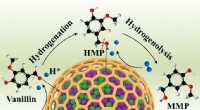 Indkapslede NiCo -legering nanopartikler, der katalyserer HDO -reaktionerEn indkapslet bimetallisk Ni-Co-legeringsstrategi er innovativt designet til at forbedre hydrodeoxygeneringsydelsen af biomassederivater til de tilsvarende methylerede produkter i vand. Kredit:Chine
Indkapslede NiCo -legering nanopartikler, der katalyserer HDO -reaktionerEn indkapslet bimetallisk Ni-Co-legeringsstrategi er innovativt designet til at forbedre hydrodeoxygeneringsydelsen af biomassederivater til de tilsvarende methylerede produkter i vand. Kredit:Chine -
 Bevægelse væk fra plastik:Etuiet med solid body washKredit:CC0 Public Domain For forbrugere, der forsøger at undgå plastik og blive grønne, solid body wash, der sælges uden emballage, ser ud til at være et godt alternativ til indpakkede og flaskes
Bevægelse væk fra plastik:Etuiet med solid body washKredit:CC0 Public Domain For forbrugere, der forsøger at undgå plastik og blive grønne, solid body wash, der sælges uden emballage, ser ud til at være et godt alternativ til indpakkede og flaskes
- Hubble tager et nærbillede af kometen NEOWISE
- Virkningerne af mikroplast på organismer i kystområder
- Hvor mange elektroner vil et svovlatom vinde eller tabe for at opnå ædelgasstruktur?
- Energiselskaber henvender sig til afslibning af dyr for at få ren strøm
- Hvad skifter varme og pres skifer til?
- Præcis tilpasning af knogleimplantater fra printeren


