Brønsted-Lowry syrer og baser:definition og nøglekarakteristika
* Syrer: Brønsted-Lowry-syrer er protondonorer . De donerer en proton (H+) til et andet molekyle eller ion.
* Baser: Brønsted-Lowry baser er protonacceptorer . De accepterer en proton (H+) fra et andet molekyle eller ion.
Eksempel:
I reaktionen af saltsyre (HCl) med vand (H2O):
* HCl (syre) + H2O (base) → H3O+ (konjugeret syre) + Cl- (konjugeret base)
* HCl donerer en proton (H+) for at danne H3O+ (hydroniumion), hvilket gør det til en syre.
* H2O accepterer en proton (H+) for at danne H3O+, hvilket gør den til en base.
Nøglepunkter:
* Brønsted-Lowry-definitionen fokuserer på protonernes bevægelse under kemiske reaktioner.
* Denne definition udvider Arrhenius-definitionen, som kun definerer syrer og baser i vandige opløsninger.
* Begrebet konjugerede syrer og baser er væsentligt i Brønsted-Lowry-teorien.
 Varme artikler
Varme artikler
-
 De mest kraftfulde og mildeste reagenser opnået baseret på miljøvenlig jodUnge forskere fra Research School of Chemistry &Applied Biomedical Sciences. Kredit:Tomsk State University Et internationalt samarbejde mellem kemikere fra Tomsk Polytekniske Universitet, USA, Sto
De mest kraftfulde og mildeste reagenser opnået baseret på miljøvenlig jodUnge forskere fra Research School of Chemistry &Applied Biomedical Sciences. Kredit:Tomsk State University Et internationalt samarbejde mellem kemikere fra Tomsk Polytekniske Universitet, USA, Sto -
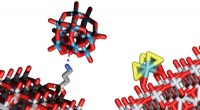 Lys i stedet for elektricitet:En ny slags grøn brintStrukturelle modeller af to klynger, der gør det muligt at spalte vand i O2 og H2 ved hjælp af lysenergi. Kredit:Vienna University of Technology Brint kan blive en vigtig del af vores fremtidige en
Lys i stedet for elektricitet:En ny slags grøn brintStrukturelle modeller af to klynger, der gør det muligt at spalte vand i O2 og H2 ved hjælp af lysenergi. Kredit:Vienna University of Technology Brint kan blive en vigtig del af vores fremtidige en -
 Returnering af nitrogen til jord uden kemikalierKredit:Flinders University Mens landbrugsproduktionen rundt om i verden kæmper med faldende jordsundhed, Australske forskere undersøger produktionen af en bæredygtig organisk nitrogengødning fre
Returnering af nitrogen til jord uden kemikalierKredit:Flinders University Mens landbrugsproduktionen rundt om i verden kæmper med faldende jordsundhed, Australske forskere undersøger produktionen af en bæredygtig organisk nitrogengødning fre -
 Forståelse af baser i kemi:definitioner, egenskaber og anvendelsershironosov/iStock/GettyImages Mens den sunde fornufts opfattelse af baser som bitre, glatte stoffer, der bliver rød lakmusblå, stadig er nyttig, er moderne kemi afhængig af kemisk adfærd for at klas
Forståelse af baser i kemi:definitioner, egenskaber og anvendelsershironosov/iStock/GettyImages Mens den sunde fornufts opfattelse af baser som bitre, glatte stoffer, der bliver rød lakmusblå, stadig er nyttig, er moderne kemi afhængig af kemisk adfærd for at klas
- Hvad er en astronomi?
- Forskere udnytter carbenernes kraft til at fremstille stoffer nemmere og mere sikkert
- Hvordan er organer form?
- Hvorfor dannes dug på græskøle nætter?
- Defekter er perfekte i laser-induceret grafen
- Hvordan bruger verden emojis? Undersøgelse finder universelle udtryk på tværs af lande og kontine…


