Ammoniak som base:Forståelse af Brønsted-Lowry-definitionen
Sådan fungerer det:
* Brønsted-Lowry Definition: Denne definition definerer en syre som en protondonor og en base som en protonacceptor.
* Ammoniak's reaktion: Når ammoniak reagerer med vand, accepterer den en proton fra et vandmolekyle og danner ammoniumionen (NH4⁺) og hydroxidionen (OH⁻):
```
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH⁻(aq)
```
* Protonaccept: Da ammoniak får en proton (H⁺) i denne reaktion, fungerer den som en base.
Nøglepunkter:
* Ammoniak's enlige elektronpar på nitrogenatomet gør det muligt for det let at acceptere en proton.
* Dannelsen af hydroxidioner (OH⁻) i reaktionen er også karakteristisk for en base.
Derfor klassificeres ammoniak som en base i henhold til Brønsted-Lowry-definitionen ud fra dens evne til at acceptere en proton.
 Varme artikler
Varme artikler
-
 Hvordan motion kan hjælpe med at bekæmpe stofmisbrugKredit:American Chemical Society Sirenekaldet fra vanedannende stoffer kan være svært at modstå, og at vende tilbage til det miljø, hvor der tidligere blev taget stoffer, kan gøre modstanden så me
Hvordan motion kan hjælpe med at bekæmpe stofmisbrugKredit:American Chemical Society Sirenekaldet fra vanedannende stoffer kan være svært at modstå, og at vende tilbage til det miljø, hvor der tidligere blev taget stoffer, kan gøre modstanden så me -
 Mikrofluidisk array fanger, holder enkelte livmoderhalsceller for hurtigere screeningEksperimentelle resultater af immunfarvede celler under anvendelse af mikrobrøndsarrayet med barrierer. Kredit:Soo Hyeon Kim Der er udviklet flere screeningstest for livmoderhalskræft i de senere
Mikrofluidisk array fanger, holder enkelte livmoderhalsceller for hurtigere screeningEksperimentelle resultater af immunfarvede celler under anvendelse af mikrobrøndsarrayet med barrierer. Kredit:Soo Hyeon Kim Der er udviklet flere screeningstest for livmoderhalskræft i de senere -
 Røntgenspredning og molekylær dynamik-simuleringer, der bruges til at skabe billeddannelse i realt…Dette billede illustrerer, at da jernoxid undergår oxidation, hulrum i nanopartiklerne smelter sammen og danner halvmåner. Kredit:Alexandra Kirby / Y. Sun et al. / Videnskab (2017) (Phys.org) –
Røntgenspredning og molekylær dynamik-simuleringer, der bruges til at skabe billeddannelse i realt…Dette billede illustrerer, at da jernoxid undergår oxidation, hulrum i nanopartiklerne smelter sammen og danner halvmåner. Kredit:Alexandra Kirby / Y. Sun et al. / Videnskab (2017) (Phys.org) – -
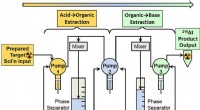 Modulært fluidsystem udviklet til at levere radioisotop, der anvendes i målrettet alfa-terapiSkematisk af opløsningsmiddelekstraktionsmodul til astatin-211 (211At) isolering fra opløst bismuth cyclotron target. Processen starter i venstre side og fortsætter til højre. Kredit:Matthew OHara, Pa
Modulært fluidsystem udviklet til at levere radioisotop, der anvendes i målrettet alfa-terapiSkematisk af opløsningsmiddelekstraktionsmodul til astatin-211 (211At) isolering fra opløst bismuth cyclotron target. Processen starter i venstre side og fortsætter til højre. Kredit:Matthew OHara, Pa
- Undersøgelse undersøger, hvordan pandemi-relaterede ændringer påvirker universitetsstuderendes m…
- Den største flyvende fugl nogensinde:En 21 fods bevinget forhistorisk kæmpe, der overskygger moder…
- Private equity-selskab køber Canadas WestJet-flyselskab
- Hvad er Johannes Kepler favorit mad?
- Forskere viser, at pesticidforurening er mere end æbleskind dyb
- Hvad er lugten af nobelium?


