Forståelse af baser i kemi:definitioner, egenskaber og anvendelser
shironosov/iStock/GettyImages
Mens den sunde fornufts opfattelse af baser som bitre, glatte stoffer, der bliver rød lakmusblå, stadig er nyttig, er moderne kemi afhængig af kemisk adfærd for at klassificere syrer og baser. Det er vigtigt at vide, hvordan baser opfører sig, fordi de reagerer med syrer for at producere salte og vand, en proces, der understøtter utallige industrielle processer og laboratorieprocesser.
TL;DR
En base er ethvert stof, der, når det opløses i vand, øger koncentrationen af hydroxidioner (OH⁻). Den oprindelige Arrhenius-definition begrænsede baser til forbindelser, der direkte producerer OH⁻, men den bredere visning fanger alle forbindelser, der hæver OH⁻-niveauer, selvom de mangler hydroxid i deres struktur.
Tidlige, empiriske definitioner
Før 1800-tallets videnskabelige revolution identificerede kemikere baser ud fra observerbare træk:bitter smag, glat følelse og evnen til at blive rødt lakmuspapir blåt. Når en syre blev tilsat, manglede det resulterende neutraliseringsprodukt - sædvanligvis et salt - begge disse egenskaber, hvilket illustrerer den komplementære natur af syrer og baser.
Arrhenius Bases (1887)
Svante Arrhenius udvidede definitionen ved at fokusere på ioner i vandige opløsninger. Han foreslog, at en base er et stof, der dissocierer i vand for at producere hydroxidioner (OH⁻) og positivt ladede ioner. Syrer blev i modsætning hertil defineret som forbindelser, der genererer hydrogenioner (H+) og negative ioner. Denne model fungerer godt til almindelige eksempler som natriumhydroxid (NaOH), der opløses i Na⁺ og OH⁻ og er klassificeret som en stærk base.
Arrhenius' struktur kan dog ikke forklare den grundlæggende opførsel af forbindelser som natriumcarbonat (Na₂CO₃). Selvom Na2CO3 mangler hydroxid i sin molekylformel, hæver det stadig OH⁻-koncentrationen i opløsning ved at reagere med vand for at danne bicarbonat- og carbonationer, som igen frigiver hydroxid. Desuden er Arrhenius' definition begrænset til vandige miljøer og udelader ikke-vandige basesyrereaktioner.
Moderne, generel definition
I dag anvender kemikere et bredere kriterium:en base er ethvert stof, der, når det opløses i et opløsningsmiddel (ikke nødvendigvis vand), øger koncentrationen af hydroxidioner i den opløsning. Syrer defineres på samme måde som stoffer, der hæver hydrogenionkoncentrationen. Denne inkluderende opfattelse omfatter alle traditionelle baser – inklusive dem, der mangler direkte OH⁻ i deres struktur – såvel som eksotiske systemer såsom Lewis-baser, der accepterer protoner eller donerer elektronpar.
At forstå disse definitioner er afgørende for at forudsige reaktionsresultater, designe industrielle processer og udføre nøjagtige laboratorieeksperimenter.
Nøgletilbehør: Baser er karakteriseret ved deres evne til at hæve hydroxidionniveauer, uanset om de selv indeholder hydroxid eller ej, og ved deres komplementære rolle til syrer i neutraliseringsreaktioner.
 Varme artikler
Varme artikler
-
 Ny metode udviklet til at udvinde antibiotikarester i fødevarer fra animalske kilderDen forsker, der er ansvarlig for undersøgelsen, Soledad González, i laboratoriet Kredit:University of Córdoba Coccidiose er en slags tarmsygdom, der rammer forskellige grupper af dyr. Det hæmmer
Ny metode udviklet til at udvinde antibiotikarester i fødevarer fra animalske kilderDen forsker, der er ansvarlig for undersøgelsen, Soledad González, i laboratoriet Kredit:University of Córdoba Coccidiose er en slags tarmsygdom, der rammer forskellige grupper af dyr. Det hæmmer -
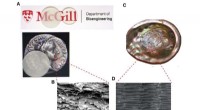 Ubrydeligt glas inspireret af muslingeskaller(A) Glaskomposit (uden indeksmatchingsstrategi til venstre og med indeksmatchning til højre), (B) Glaskomposits mikrostruktur, (C) Udsigt over det nacreøse lag i rød abalone shell, og (D) Nacres mikro
Ubrydeligt glas inspireret af muslingeskaller(A) Glaskomposit (uden indeksmatchingsstrategi til venstre og med indeksmatchning til højre), (B) Glaskomposits mikrostruktur, (C) Udsigt over det nacreøse lag i rød abalone shell, og (D) Nacres mikro -
 Hvorfor bliver nogle legeringer stærkere ved stuetemperatur?Kredit:Pixabay/CC0 Public Domain En legering er typisk et metal, hvor der er tilføjet nogle få procent af mindst ét andet element. Nogle aluminiumslegeringer har en tilsyneladende mærkelig egens
Hvorfor bliver nogle legeringer stærkere ved stuetemperatur?Kredit:Pixabay/CC0 Public Domain En legering er typisk et metal, hvor der er tilføjet nogle få procent af mindst ét andet element. Nogle aluminiumslegeringer har en tilsyneladende mærkelig egens -
 Motion er godt for din hud:Et protein efterligner nogle antialdringseffekter hos musForskere forstår endnu ikke virkningerne af aldring på de cellulære processer, der er involveret i hudheling. Justin Crane, en assisterende professor i biologi på Northeastern, og Wesley Wong, en fjer
Motion er godt for din hud:Et protein efterligner nogle antialdringseffekter hos musForskere forstår endnu ikke virkningerne af aldring på de cellulære processer, der er involveret i hudheling. Justin Crane, en assisterende professor i biologi på Northeastern, og Wesley Wong, en fjer
- Sådan slår du specifikke gener til og fra
- Er bisoprolol og fumarat det samme?
- Bringer realtid, finskala, kvalitetskontrol under overfladen til 3D -udskrivning
- Forskere bruger maskinlæringsmodelleringsværktøjer til at forbedre zink-finger-nuklease-redigerin…
- Hvordan påvirker erosion og deponering landformer?
- CGCS 673 er en semi-regulær variabel kulstofstjerne, undersøgelse finder


