Lokalisering af halvækvivalenspunktet på en titreringskurve:en praktisk vejledning
Af Chris Deziel | Opdateret 24. marts 2022
Under en typisk syre-base titrering plottes den udviklende pH mod mængden af tilsat titrant. Den resulterende kurve starter med en gradvis stigning og stejler derefter kraftigt ved ækvivalenspunktet, hvor al syre er blevet neutraliseret. Punktet nøjagtigt halvvejs mellem oprindelsen og ækvivalenspunktet på x-aksen er halvækvivalenspunktet. På dette tidspunkt er opløsningens pH lig med syrens dissociationskonstant, pKa.
Placering af halvækvivalenspunktet
Titreringen overvåges ved hjælp af en farveskiftende indikator, et pH-meter, et potentiometer eller spektroskopiske teknikker. Efterhånden som basen tilsættes, stiger pH-værdien langsomt, indtil den når ækvivalenspunktet; ud over det stiger kurven stejlt. Efter ækvivalensvolumenet aftager hældningen igen, og pH stiger mere gradvist.
Identificer ækvivalenspunktet ved at lokalisere bøjningen, hvor kurven går fra den blide til den stejle skråning. Når det volumen er kendt, er halv-ækvivalenspunktet simpelthen midtpunktet på x-aksen mellem nulvolumen og ækvivalensvolumenet.
Betydningen af det halve ækvivalenspunkt
Henderson-Hasselbalch-ligningen, pH =pKa + log([A⁻]/[HA]), forbinder syre-base-forholdet til pH. Ved halvækvivalenspunktet er koncentrationerne af syren (HA) og dens konjugatbase (A⁻) ens, hvilket gør forholdet til et. Følgelig er log1 =0, og ligningen reduceres til pH =pKa. Ved at tegne en lodret linje til halvækvivalensvolumenet og en vandret linje til y-aksen kan pKa derfor aflæses direkte fra kurven.
At kende halvækvivalenspunktet er afgørende for at karakterisere svage syrer, designe buffersystemer og validere titreringsprotokoller.
 Varme artikler
Varme artikler
-
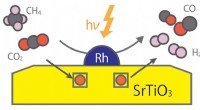 Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky
Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky -
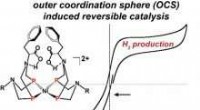 Forskere designer hurtigt, reversible bio-inspirerede katalysatorerKredit:Environmental Molecular Sciences Laboratory For at vind- og solkraft kan blive grundpillerne i vedvarende energi, den energi, de producerer med mellemrum, skal lagres og hentes effektivt. O
Forskere designer hurtigt, reversible bio-inspirerede katalysatorerKredit:Environmental Molecular Sciences Laboratory For at vind- og solkraft kan blive grundpillerne i vedvarende energi, den energi, de producerer med mellemrum, skal lagres og hentes effektivt. O -
 Brækker rumaffald nogensinde naturligt ned? (video)Kan du huske, da Elon Musk sendte en bil ud i rummet? Den bil driver ikke bare fredeligt gennem et vakuum – den suser rundt om solen med 63.592 miles i timen og bliver bombarderet af solstråling. Det
Brækker rumaffald nogensinde naturligt ned? (video)Kan du huske, da Elon Musk sendte en bil ud i rummet? Den bil driver ikke bare fredeligt gennem et vakuum – den suser rundt om solen med 63.592 miles i timen og bliver bombarderet af solstråling. Det -
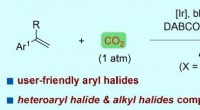 Synligt lys-drevet arylcarboxylering af styrener med kuldioxid og arylhalogeniderFigur:Synligt lys-drevet arylcarboxylering af styrener med CO2 og arylhalogenider. Kredit:Prof. LIs gruppe Brugen af kuldioxid (CO 2 ), som er en ideel one-carbon (C1) byggesten og er bæredygt
Synligt lys-drevet arylcarboxylering af styrener med kuldioxid og arylhalogeniderFigur:Synligt lys-drevet arylcarboxylering af styrener med CO2 og arylhalogenider. Kredit:Prof. LIs gruppe Brugen af kuldioxid (CO 2 ), som er en ideel one-carbon (C1) byggesten og er bæredygt
- Hvornår opdagede Aristoteles, at Jupiter Moons og der hvor bjerge på månen?
- På hvilket tidspunkt har den sydlige halvkugle største eksponering for sol?
- Hvordan har NASA hjulpet med at forbedre vores luft og vand?
- Billede:Hubbles kosmiske feriekrans
- Hvad er årslønnen for en kemiker?
- Hvad er ligningen for at finde ud af vægten?


