Forskere bruger maskinlæringsmodelleringsværktøjer til at forbedre zink-finger-nuklease-redigeringsteknologi
Genom redigering gør indhug i biomedicinsk forskning og medicin. Ved at anvende værktøjer til biomolekylemodellering accelererer et japansk forskerhold tempoet og reducerer omkostningerne ved zinkfingernuklease (ZFN) teknologi, et primært genredigeringsværktøj.
I en undersøgelse offentliggjort i Advanced Science , forskere fra Hiroshima University og det japanske nationale institut for avanceret industriel videnskab og teknologi demonstrerer, hvordan maskinlæringsdrevne modulære samlingssystemer kan forbedre genredigering.
"Genomredigering er et lovende værktøj til behandling af genetiske lidelser på en række forskellige områder," sagde Shota Katayama, lektor i Genome Editing Innovation Center ved Hiroshima University. "Ved at forbedre effektiviteten af genredigeringsteknologier kan vi opnå større præcision i modifikationer af den genetiske information i levende celler."
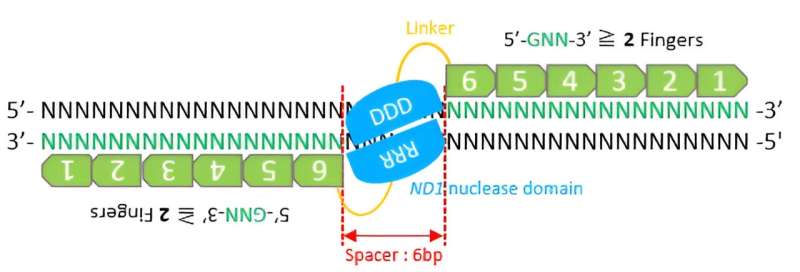
Ved siden af CRISPR/Cas9 og TALEN er zinkfingernuklease et vigtigt værktøj inden for genomredigering. Konstrueret til at bryde visse bindinger inden for polynukleotidkæden af et DNA-molekyle, består disse kimære proteiner af to domæner fusioneret sammen:DNA-bindings- og DNA-spaltningsdomæner. Det zinkfinger-proteinbindende domæne (ZF) genkender den målrettede DNA-sekvens i det komplette genom, mens spaltningsdomænet involverer et særligt DNA-skærende enzym kaldet ND1-endonukleaser.
ZFN'er præsenterer et par fordele i forhold til CRISPR/Cas9 og TALEN:For det første, i modsætning til CRISPR-Cas9, er patenterne for ZFN'er allerede udløbet, hvilket udelukker høje patent royalties for industrielle applikationer. For det andet er ZFN'er mindre, hvilket gør det muligt for ZFN-kodende DNA let at blive pakket ind i en viral vektor med begrænset lastplads til in vivo og kliniske applikationer.
For at skære DNA skal to ZFN'er være bundet. Derfor skal de designes i par for at være funktionelle på ethvert nyt sted. Det har imidlertid vist sig udfordrende at konstruere funktionelle ZFN'er og forbedre deres genomredigeringseffektivitet.
"Vi har gjort store fremskridt med metoder til at udlede zink-fingersæt til nye genomiske mål, men der er stadig plads til at forbedre vores tilgange til design og udvælgelse," sagde Katayama.
Selektionsbaserede metoder kan bruges til at konstruere samlede ZF-proteiner, men disse metoder er arbejdskrævende og tidskrævende. En alternativ fremgangsmåde til at konstruere samlede ZF-proteiner er samlingen af ZF-moduler ved hjælp af standard molekylærbiologiske teknikker. Denne metode giver forskerne en meget nemmere metode til at konstruere samlede ZF-proteiner.
Imidlertid har modulært sammensatte ZFN'er et lille antal funktionelle ZFN-par med en fejlrate på 94 % for de testede ZFN-par.
I deres undersøgelse sigtede forskerne fra Hiroshima University og det japanske nationale institut for avanceret industriel videnskab og teknologi efter at skabe en mere effektiv, let konstruerbar zinkfingernuklease til genredigering ved hjælp af offentligt tilgængelige ressourcer i et modulært samlingssystem.
En vigtig overvejelse i designet af ZFN'er er antallet af zinkfingre, der kræves for effektiv og specifik spaltning. Holdet antog, at den modulære samling af ZF-modulerne ville være nyttig til at konstruere ZFN'er med fem eller seks fingre.
I deres publikation præsenterede forskerholdet en metode til at øge effektiviteten af konstruktionen af funktionelle ZFN'er og forbedringen af deres genomredigeringseffektivitet ved hjælp af tre biomolekylemodelleringsværktøjer:AlphaFold, Coot og Rosetta.
Af de 10 testede ZFN'er opnåede forskerne to funktionelle par. Desuden øgede konstruktionen af ZFN'er ved hjælp af AlphaFold, Coot og Rosetta effektiviteten af genomredigering med 5 %, hvilket demonstrerer effektiviteten af konstruktion af ZFN'er baseret på strukturel modellering.
Flere oplysninger: Shota Katayama et al., Engineering af zinkfingernukleaser gennem strukturel modellering forbedrer effektiviteten af genomredigering i celler, Avanceret videnskab (2024). DOI:10.1002/advs.202310255
Journaloplysninger: Avanceret videnskab
Leveret af Hiroshima University
 Varme artikler
Varme artikler
-
 Kan data redde delfiner? Hvordan videnskabsmænd bruger NASA-data til at studere sammenhængen melle…Illustration af en atlantisk hvidsidet delfin og en langfinnet grindehval, to havpattedyrarter, der strander i Cape Cod. Kredit:NASA GSFC/CIL/Brian Monroe Det ældgamle mysterium om, hvorfor ellers
Kan data redde delfiner? Hvordan videnskabsmænd bruger NASA-data til at studere sammenhængen melle…Illustration af en atlantisk hvidsidet delfin og en langfinnet grindehval, to havpattedyrarter, der strander i Cape Cod. Kredit:NASA GSFC/CIL/Brian Monroe Det ældgamle mysterium om, hvorfor ellers -
 Ny undersøgelse afslører mekanismer for, hvordan sygdomsspredende prioner kan hoppe fra en art til…Dette mikrofotografi af hjernevæv afslører de cytoarkitektoniske histopatologiske ændringer fundet i bovin spongiform encephalopati. Tilstedeværelsen af vakuoler, det vil sige mikroskopiske huller i
Ny undersøgelse afslører mekanismer for, hvordan sygdomsspredende prioner kan hoppe fra en art til…Dette mikrofotografi af hjernevæv afslører de cytoarkitektoniske histopatologiske ændringer fundet i bovin spongiform encephalopati. Tilstedeværelsen af vakuoler, det vil sige mikroskopiske huller i -
 Hvordan poliovirus overtager celler indefraDet venstre billede viser, hvordan nydannede polioviruspartikler (lyserøde) er fyldt med virusgenomet og bliver til infektiøse vira (røde). Til højre:hvis cellens protein VPS34 hæmmes, stopper virussa
Hvordan poliovirus overtager celler indefraDet venstre billede viser, hvordan nydannede polioviruspartikler (lyserøde) er fyldt med virusgenomet og bliver til infektiøse vira (røde). Til højre:hvis cellens protein VPS34 hæmmes, stopper virussa -
 Bruger du virkelig kun 10 procent af din hjerne?Denne mand kan ikke finde ud af, hvorfor vi kun ville bruge 10 procent af vores hjerner. Se flere hjernebilleder. Chris Ryan/OJO Images Ltd/Getty Images Chancerne er, på et eller andet tidspunkt, nog
Bruger du virkelig kun 10 procent af din hjerne?Denne mand kan ikke finde ud af, hvorfor vi kun ville bruge 10 procent af vores hjerner. Se flere hjernebilleder. Chris Ryan/OJO Images Ltd/Getty Images Chancerne er, på et eller andet tidspunkt, nog
- En rekord tæt barbering:Asteroid 2020 VT4 lige skummet af Jorden
- Opdager nye partikler ved hjælp af sorte huller
- Sådan finder du Salg Price
- Undslippende kinetiske fælder:Hvordan molekylære interaktioner gør det muligt at overvinde energi…
- Sådan starter du en præsentation om Fast Food
- Undersøgelse afslører det ændrede omfang af indianske grundvandsrettigheder


