Beregning af molær masse:inklusive krystallisationsvand
Her er hvorfor:
* Krystallisationsvand er vandmolekyler, der er inkorporeret i krystalstrukturen af en forbindelse.
* Disse vandmolekyler er kemisk bundet til forbindelsen og bidrager til dens samlede masse.
* Molar masse er massen af et mol af et stof. Det inkluderer massen af alle atomerne i forbindelsen, inklusive krystallisationsvandet.
Eksempel:
* Kobber(II)sulfatpentahydrat (CuSO₄·5H₂O) har fem vandmolekyler pr. formelenhed.
* For at beregne dens molære masse skal du inkludere massen af disse vandmolekyler sammen med massen af kobber-, svovl- og oxygenatomerne.
Lad mig vide, hvis du gerne vil have et specifikt eksempel udarbejdet!
Sidste artikelCs₂O-formel:Forståelse af cæsiumoxiddannelse
Næste artikelCH3-CH2-CH3 vs. Pentan:Forstå forskellen
 Varme artikler
Varme artikler
-
 Nye materialer:Strålende hvid uden pigmenterEn nanostruktureret polymerfilm modelleret efter den hvide bille Cyphochilus insulanus producerer en strålende hvid belægning. Kredit:Julia Syurik, KIT Polymerfolier, der er ekstremt tynde og kend
Nye materialer:Strålende hvid uden pigmenterEn nanostruktureret polymerfilm modelleret efter den hvide bille Cyphochilus insulanus producerer en strålende hvid belægning. Kredit:Julia Syurik, KIT Polymerfolier, der er ekstremt tynde og kend -
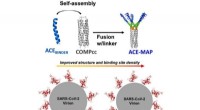 Konstrueret multivalent selvsamlet bindeprotein mod SARS-CoV-2 RBDGrafisk abstrakt. Kredit:Biochemical Engineering Journal (2022). DOI:10.1016/j.bej.2022.108596 Siden den dukkede op i 2019, har COVID-19 krævet over 6 millioner liv og vendt samfundet over hele klo
Konstrueret multivalent selvsamlet bindeprotein mod SARS-CoV-2 RBDGrafisk abstrakt. Kredit:Biochemical Engineering Journal (2022). DOI:10.1016/j.bej.2022.108596 Siden den dukkede op i 2019, har COVID-19 krævet over 6 millioner liv og vendt samfundet over hele klo -
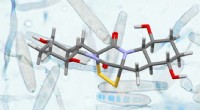 En ny strategi for syntese af komplekse naturlige produkterStruktur af Rostratin A (forgrund) og svampen exserohilum rostratum, hvorfra den blev isoleret (baggrund). Kredit:Universitetet i Basel, Olivier Baudoin mit Erlaubnis af G. Roberts Det er lykkedes
En ny strategi for syntese af komplekse naturlige produkterStruktur af Rostratin A (forgrund) og svampen exserohilum rostratum, hvorfra den blev isoleret (baggrund). Kredit:Universitetet i Basel, Olivier Baudoin mit Erlaubnis af G. Roberts Det er lykkedes -
 Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors
Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors
- Hvilke elementer laver jernpyrit?
- Lyskasse fra 500 år siden fundet i smeltende gletsjer i Norge
- Kan det virkelig betale sig at være vært for OL, VM eller andre store sportsbegivenheder?
- Hvad og hvor er den 126. planet?
- Hvem opfandt røntgenstrålen?
- Størrelsen af en naturbrand i Oregon understreger det store vestlige USA


