Hybridisering af Cl2O:En trin-for-trin guide
1. Tegn Lewis-strukturen
* Tæl valenselektroner: Klor (Cl) har 7 valenselektroner, og ilt (O) har 6. Med to kloratomer er det samlede antal 7 + 7 + 6 =20 valenselektroner.
* Forbind atomerne: Placer iltatomet i midten, da det er mindre elektronegativt. Forbind det til de to kloratomer med enkeltbindinger.
* Fuldstændige oktetter: Hvert kloratom har brug for 6 elektroner mere, og iltatomet har brug for 4 mere. Dette kræver to ensomme par på hvert kloratom og to enlige par på iltatomet.
2. Bestem det steriske nummer
* Sterisk nummer: Dette er antallet af elektrongrupper omkring det centrale atom. Elektrongrupper omfatter bindinger (enkelt, dobbelt eller tredobbelt) og enlige par.
* I Cl₂O: Oxygenatomet har to bindinger (til kloratomerne) og to ensomme par, hvilket giver det et sterisk tal på 4.
3. Relater sterisk nummer til hybridisering
* Sterisk nummer | Hybridisering
* 2 | sp
* 3 | sp²
* 4 | sp³
* 5 | sp³d
* 6 | sp³d²
4. Konklusion
Da det centrale oxygenatom i Cl2O har et sterisk tal på 4, er dets hybridisering sp³ .
Sidste artikelHybridisering af ClO3-:En trin-for-trin guide
Næste artikelSO2-hybridisering:En detaljeret forklaring med Lewis-strukturen
 Varme artikler
Varme artikler
-
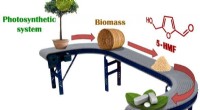 Grønnere medicinalindustrienDen nye proces er attraktiv, fordi den neutraliserer kulstof, som bidrager til globale klimaforandringer. Kredit:Zelinsky Institute of Organic Chemistry Syntetisering af livreddende lægemidler fra
Grønnere medicinalindustrienDen nye proces er attraktiv, fordi den neutraliserer kulstof, som bidrager til globale klimaforandringer. Kredit:Zelinsky Institute of Organic Chemistry Syntetisering af livreddende lægemidler fra -
 Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u
Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u -
 Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin
Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin -
 Forskere skaber nye kemiske næser for at befri miljøet for industrielle forurenende stofferTegneseriebillede af den kemiske næse. Kredit:Prof Riina Aav Forskere fra fem europæiske lande er gået sammen om at udvikle næste generations kemiske næser for at fjerne industrielle forurenende s
Forskere skaber nye kemiske næser for at befri miljøet for industrielle forurenende stofferTegneseriebillede af den kemiske næse. Kredit:Prof Riina Aav Forskere fra fem europæiske lande er gået sammen om at udvikle næste generations kemiske næser for at fjerne industrielle forurenende s
- Hvad bruges instrumentet til måling af frekvens?
- Hvordan gamle afgrøder kunne modvirke klimaændringseffekter
- Fremskridt i topologisk faseovergang i organometalliske gitter
- Deepfakes kaldte ny valgtrussel, uden let løsning
- At bruge en mobil, mens de surfer på hylderne, kan få kunderne til at købe mere
- Profilering af ekstreme stråler:Forskere udtænker ny diagnostik til banebrydende og næste generat…


