Afbalancering af kemiske ligninger:Forståelse af koefficienter og nedskrivninger
Her er hvorfor:
* Koefficienter repræsenterer antallet af mol af hver reaktant og produkt. Ændring af koefficienten ændrer mængden af hvert stof involveret i reaktionen.
* Underskrifter i kemiske formler angiver antallet af atomer af hvert grundstof i et molekyle. Du kan ikke ændre subscripts for at balancere en ligning, da det ville ændre identiteten af selve molekylet.
Eksempel:
Ubalanceret ligning:H₂ + O₂ → H₂O
Balanceret ligning:2H₂ + O₂ → 2H2O
I dette eksempel tilføjede vi en koefficient på "2" foran både H₂ og H₂O. Dette sikrer, at vi har det samme antal brint- og oxygenatomer på begge sider af ligningen (4 brintatomer og 2 oxygenatomer).
Nøgleprincip:
Loven om bevarelse af masse dikterer, at i en kemisk reaktion skal den samlede masse af reaktanterne svare til den samlede masse af produkterne. Afbalancering af ligninger sikrer, at antallet af atomer i hvert grundstof forbliver det samme på begge sider, hvilket opfylder loven om bevarelse af masse.
 Varme artikler
Varme artikler
-
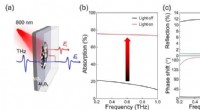 Forskere opfinder bredbånds afstembar terahertz-absorber(a) Skematisk THz-pulsudbredelse gennem VO2-filmen på Al2O3-substratet. (b) Målte ændringen af THz-absorption af VO2-film med og uden lys. (c) Målte ændringen af THz-refleksion og reflektionsfasef
Forskere opfinder bredbånds afstembar terahertz-absorber(a) Skematisk THz-pulsudbredelse gennem VO2-filmen på Al2O3-substratet. (b) Målte ændringen af THz-absorption af VO2-film med og uden lys. (c) Målte ændringen af THz-refleksion og reflektionsfasef -
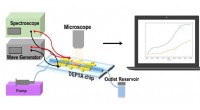 Forskere udvikler et laboratorium på en chip til personlig overvågning af lægemiddeleffektivitetKredit:University of California, Irvine UCI forskere og samarbejdspartnere har udviklet en lab on a chip platform for at lette kontinuerlige, billig, hurtig og personlig lægemiddelscreening. Tekno
Forskere udvikler et laboratorium på en chip til personlig overvågning af lægemiddeleffektivitetKredit:University of California, Irvine UCI forskere og samarbejdspartnere har udviklet en lab on a chip platform for at lette kontinuerlige, billig, hurtig og personlig lægemiddelscreening. Tekno -
 Menneskehår bruges til at lave fleksible skærme til smarte enhederKredit:Queensland University of Technology Forskere fra Queensland University of Technology og Griffith University har udviklet en metode til at forvandle små hårstrå til carbon nanodots, som er s
Menneskehår bruges til at lave fleksible skærme til smarte enhederKredit:Queensland University of Technology Forskere fra Queensland University of Technology og Griffith University har udviklet en metode til at forvandle små hårstrå til carbon nanodots, som er s -
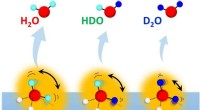 Indvirkningen af molekylær rotation på en ejendommelig isotopeffekt på vandhydrogenbindingerDesorption af vandisotopomerer (H 2 Åh, HDO og D 2 O) fra overflader af isotopblandet is med forskellige H/D-sammensætninger. Kredit:NINS/IMS Kvantenaturen af brintbindinger i vand manifeste
Indvirkningen af molekylær rotation på en ejendommelig isotopeffekt på vandhydrogenbindingerDesorption af vandisotopomerer (H 2 Åh, HDO og D 2 O) fra overflader af isotopblandet is med forskellige H/D-sammensætninger. Kredit:NINS/IMS Kvantenaturen af brintbindinger i vand manifeste
- Forskere forklarer synligt lys fra 2-D blyhalogenidperovskitter
- Hvad er den konstante ændring i form og struktur af klipper kaldet?
- Hvordan kinesiske virksomheder drager fordel af mangfoldigheden af udenlandske direkte investering…
- Hvad er forskellen mellem en diploid celle og haploid?
- Udøver en lav pH negativ feedback på produktionen af cholecystokinin eller gastrin?
- Har bølger med de korteste bølgelængder højeste frekvenser?


