Indvirkningen af molekylær rotation på en ejendommelig isotopeffekt på vandhydrogenbindinger
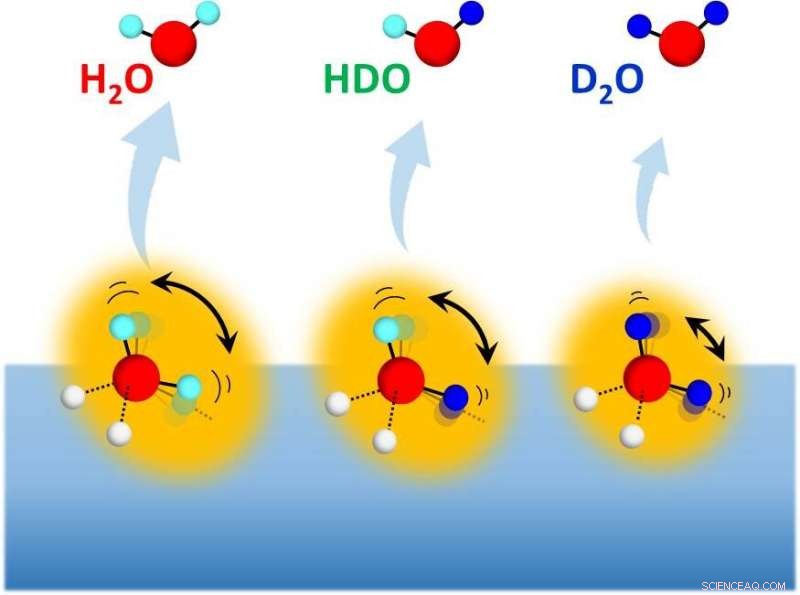
Desorption af vandisotopomerer (H 2 Åh, HDO og D 2 O) fra overflader af isotopblandet is med forskellige H/D-sammensætninger. Kredit:NINS/IMS
Kvantenaturen af brintbindinger i vand manifesterer sig i ejendommelige fysisk-kemiske isotopeffekter:Mens deuteration ofte forlænger og svækker hydrogenbindinger af typiske hydrogenbundne systemer sammensat af voluminøse molekyler, det forlænger, men styrker hydrogenbindinger af vandmolekylære aggregater. Oprindelsen af denne unikke isotopeffekt af vandmolekyler mangler at blive belyst på molekylært niveau. En nylig eksperimentel undersøgelse af sublimering af isotopblandet vandis har løst dette problem.
De fysisk-kemiske og biologiske egenskaber af hydrogenbundne systemer er væsentligt påvirket af nukleare kvanteeffekter, herunder nulpunktsenergier af vibrationstilstande, proton delokalisering, og tunneleffekt. Disse stammer fra brints ekstremt lave kernemasse; dermed, hydrogenbundne systemer viser bemærkelsesværdige isotopvirkninger ved deuteration. I 1930'erne, Ubbelohde foreslog først, at deuteration forlænger og svækker hydrogenbindinger i mange hydrogenbundne systemer. Lige siden, en sådan isotopeffekt er blevet bekræftet bredt og er i dag kendt som Ubbelohde-effekten. I modsætning, deutererende vandmolekyler i flydende vand og is forlænges, men styrker brintbindinger. På trods af intensive eksperimentelle og teoretiske undersøgelser i mere end trekvart århundrede, oprindelsen på molekylært niveau af denne særlige isotopeffekt på vandhydrogenbindinger har været uklar.
For nylig, forskere ledet af Toshiki Sugimoto, lektor ved Institut for Molekylær Videnskab, har tacklet det mangeårige mysterium:Hvordan kan mere udvidet D 2 O-aggregater danner stærkere hydrogenbindinger end H 2 O tilslag, i modsætning til de hydrogenbundne systemer, der består af voluminøse molekyler? Ved hjælp af isotopselektive målinger på sublimering af isotopblandet is med forskellige H/D isotopsammensætninger, forskerne har gjort en ny opdagelse for at opklare mysteriet; isotopeffekten på styrken af brintbindinger er styret af to deuterationseffekter:(1) den bindingsforstærkende effekt afledt af nulpunktsenergi fra hindret rotationsbevægelse, og (2) den bindingssvækkende (og forlængende) effekt afledt af kvanteanharmonisk kobling mellem inter- og intramolekylære tilstande.
Det vigtigste koncept er, at deuterationseffekten (1) afledt af rotationsbevægelse spiller afgørende roller i bindingsbrudsprocessen for ekstremt små og lette molekyler. I tilfælde af vandtilslag, enorm isotopisk forskel i nulpunktsenergien for hindret rotation frembringer en ejendommelig karakter af den bindingsforstærkende effekt (1), der er overvældende over den bindingssvækkende effekt (2), fører til den unikke isotopeffekt:deutererede vandmolekyler danner længere, men stærkere brintbindinger end hydrogenerede vandmolekyler. I modsætning, i tilfælde af andre typiske hydrogenbundne systemer sammensat af større og tungere molekyler, såsom oxalsyredihydrat, benzoesyre, ravsyre, og cyclohexan/Rh(111), de isotopiske forskelle i nulpunktsenergien for hindret rotation er ubetydeligt små. Derfor, kun den bindingssvækkende effekt (2) er fremherskende i isotopeffekten på deres bindingsenergi, hvilket resulterer i de længere og svagere hydrogenbindinger i deutererede systemer end hydrogenerede systemer. Dermed, de isotopiske forskelle i styrken af hydrogenbindinger bestemmes af en delikat balance mellem de konkurrerende to deuterationseffekter (1) og (2), mens dem i brintbindingslængde, dvs. geometrisk isotopeffekt, er dybest set domineret af deuterationseffekten (2).
"Disse resultater og koncepter giver et nyt grundlag for vores grundlæggende forståelse af de stærkt kvantevandshydrogenbindinger, " siger Sugimoto.
Sidste artikelEn legering, der bevarer sin hukommelse ved høje temperaturer
Næste artikelTo chirale katalysatorer arbejder hånd i hånd
 Varme artikler
Varme artikler
-
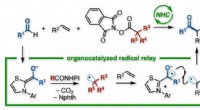 Vicinal reaktion:En radikal strategi for sammenkædning af tre organiske grupperEt japansk forskerteam ved Kanazawa University udviklede en reaktion for at skabe funktionaliserede ketoner. Ved hjælp af en N-heterocyklisk carbene (NHC) organokatalysator, uden behov for metaller el
Vicinal reaktion:En radikal strategi for sammenkædning af tre organiske grupperEt japansk forskerteam ved Kanazawa University udviklede en reaktion for at skabe funktionaliserede ketoner. Ved hjælp af en N-heterocyklisk carbene (NHC) organokatalysator, uden behov for metaller el -
 Nyt værktøj kunne behandle blodinfektioner hurtigtKredit:CC0 Public Domain Blodbaneinfektioner er notorisk dødelige. Ikke fordi de ikke kan behandles, men fordi de arbejder hurtigt og er svære at diagnosticere. For at finde ud af, hvilken medicin
Nyt værktøj kunne behandle blodinfektioner hurtigtKredit:CC0 Public Domain Blodbaneinfektioner er notorisk dødelige. Ikke fordi de ikke kan behandles, men fordi de arbejder hurtigt og er svære at diagnosticere. For at finde ud af, hvilken medicin -
 Masseproduktion af individualiserede produkterRobot-assisteret inkjet print på 3D overflader hos Fraunhofer ENAS. Kredit:Biermann&Jung Hvordan kan masseproduktionsmetoder anvendes på individualiserede produkter? Et svar er at bruge en kombina
Masseproduktion af individualiserede produkterRobot-assisteret inkjet print på 3D overflader hos Fraunhofer ENAS. Kredit:Biermann&Jung Hvordan kan masseproduktionsmetoder anvendes på individualiserede produkter? Et svar er at bruge en kombina -
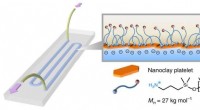 Bro over koblede farvande:Forskere 3-D-printer laboratorium med fuld væske på en chipNår to væsker - den ene indeholder nanoskala lerpartikler, en anden indeholdende polymerpartikler - er trykt på et glassubstrat, de kommer sammen ved grænsefladen mellem de to væsker og danner inden f
Bro over koblede farvande:Forskere 3-D-printer laboratorium med fuld væske på en chipNår to væsker - den ene indeholder nanoskala lerpartikler, en anden indeholdende polymerpartikler - er trykt på et glassubstrat, de kommer sammen ved grænsefladen mellem de to væsker og danner inden f
- Planter og dyr i den sydvestlige ørken
- Hvad er normativ og beskrivende videnskab?
- Nye molekyler afledt af cannabidiol er designet med mere potente antioxidanter
- Forskning undersøger for første gang fordelene og omkostningerne ved nye vandgenbrugssystemer
- Bælgfrugter til en bæredygtig landbrugs fremtid
- Målretning mod kræftceller med nanopartikler


