Eksotermiske reaktioner:Forståelse af ΔH og varmeafgivelse
Sådan fungerer det:
* Eksoterm reaktion: ΔH er negativ . Det betyder, at der frigives varme fra systemet til omgivelserne.
* Endoterm reaktion: ΔH er positiv . Det betyder, at varme absorberes af systemet fra omgivelserne.
Eksempel:
Forbrænding af metan (exoterm):
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔH =-890 kJ/mol
Den negative ΔH indikerer, at der frigives 890 kJ varme pr. mol brændt metan.
Vigtig bemærkning:
Mens ΔH er den mest almindelige indikator, kan du også bruge andre faktorer til at bestemme, om en reaktion er eksoterm, som:
* Temperaturstigning: Hvis temperaturen i omgivelserne stiger under reaktionen, er den sandsynligvis eksoterm.
* Udgivelse af lys eller varme: At observere en flamme eller føle varme genereret under reaktionen tyder på eksoterm adfærd.
Husk, at nøglen er at se efter tegn på varme, der frigives fra systemet, som er den definerende egenskab for en eksoterm reaktion.
 Varme artikler
Varme artikler
-
 Belysning af de elektroniske egenskaber ved enkeltvæggede kulstof nanohorn(a) TEM-billede af dahlia-formede SWCNH-bundter. Skalaen er 50 nm. (b) Raman-spektre af SWCNHer, exciteret med en 532 nm laser. Kredit:European Research Institute of Catalysis Enkeltvæggede kulstof
Belysning af de elektroniske egenskaber ved enkeltvæggede kulstof nanohorn(a) TEM-billede af dahlia-formede SWCNH-bundter. Skalaen er 50 nm. (b) Raman-spektre af SWCNHer, exciteret med en 532 nm laser. Kredit:European Research Institute of Catalysis Enkeltvæggede kulstof -
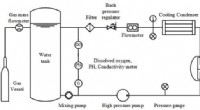 Forskere opnår nye resultater om korrosionsadfærd af legeringsmaterialer under ekstreme miljøerFig. 1. Skematisk diagram af højtemperatur- og højtryksvanddynamisk korrosionsanordning. Kredit:LIU Chao Materialers serviceadfærd under ekstreme miljøer er en af flaskehalsene, der begrænser ud
Forskere opnår nye resultater om korrosionsadfærd af legeringsmaterialer under ekstreme miljøerFig. 1. Skematisk diagram af højtemperatur- og højtryksvanddynamisk korrosionsanordning. Kredit:LIU Chao Materialers serviceadfærd under ekstreme miljøer er en af flaskehalsene, der begrænser ud -
 Forskere finder en måde at skrælle slimede biofilm som gamle klistermærkerKredit:Princeton University Slimet, svært at rengøre bakteriemåtter kaldet biofilm forårsager problemer lige fra medicinske infektioner til tilstoppede afløb og tilsmudset industriudstyr. Nu, fors
Forskere finder en måde at skrælle slimede biofilm som gamle klistermærkerKredit:Princeton University Slimet, svært at rengøre bakteriemåtter kaldet biofilm forårsager problemer lige fra medicinske infektioner til tilstoppede afløb og tilsmudset industriudstyr. Nu, fors -
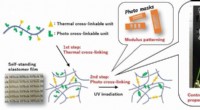 Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk
Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk


