Forudsigelse af produkter af metal-syre-reaktioner:Carbonater og oxider
Forstå reaktionerne
* Metaller med syrer: Dette er en enkelt forskydningsreaktion, hvor et metal (typisk mere reaktivt end brint) fortrænger hydrogen fra en syre.
* Metalcarbonater med syrer: Syren reagerer med carbonatet for at producere kuldioxidgas, vand og et salt.
* Metaloxider med syrer: Syren reagerer med oxidet og danner vand og et salt.
Forudsigelse af produkterne
1. Identificer reaktanterne:
* Metal: Metallet vil være elementsymbolet (f.eks. Mg, Zn, Fe).
* Syre: Almindelige syrer omfatter saltsyre (HCl), svovlsyre (H2SO4) og salpetersyre (HNO3).
* Metalkarbonat: Carbonatet vil have formlen M2CO3 (hvor M repræsenterer metallet).
* Metaloxid: Oxidet vil have formlen MO (hvor M repræsenterer metallet).
2. Identificer produkterne:
* Metaller + Syrer:
* Salt: Saltet vil blive dannet af metalkationen og syrens anion. For eksempel:
* Mg + HCl → MgCl2 + H2 (Magnesiumchlorid)
* Zn + H₂SO4 → ZnSO4 + H₂ (zinksulfat)
* Metalcarbonater + syrer:
* Salt: Saltet vil blive dannet af metalkationen og syrens anion.
* kuldioxid: CO₂ (gas)
* Vand: H2O
* CaCO3 + 2HCl → CaCl2 + CO₂ + H2O (Calciumchlorid)
* Na₂CO3 + H₂SO4 → Na₂SO4 + CO₂ + H2O (natriumsulfat)
* Metaloxider + syrer:
* Salt: Saltet vil blive dannet af metalkationen og syrens anion.
* Vand: H2O
* CuO + 2HNO₃ → Cu(NO₃)₂ + H2O (kobber(II)nitrat)
* Fe2O3 + 3H₂SO4 → Fe₂(SO4)3 + 3H₂O (jern(III)sulfat)
Afbalancering af de kemiske ligninger
Efter at have identificeret produkterne, skal du sørge for, at den kemiske ligning er afbalanceret ved at justere koefficienterne (tallene foran hver kemisk formel), så antallet af atomer i hvert grundstof er det samme på begge sider af ligningen.
Vigtige overvejelser
* Reaktivitet: Ikke alle metaller reagerer med alle syrer. Metallets reaktivitet og syrens styrke spiller en rolle. Du kan henvise til en reaktivitetsserie af metaller for at forudsige, om en reaktion vil forekomme.
* Opløselighed: De dannede salte kan være opløselige eller uopløselige i vand.
Eksempel:
Lad os forudsige produkterne af reaktionen mellem zinkmetal og svovlsyre:
1. Reaktanter: Zn (zink), H2SO4 (svovlsyre)
2. Produkter: ZnSO4 (zinksulfat), H2 (brintgas)
3. Balanceret ligning: Zn + H2S04 -> ZnSO4 + H2
Sig til, hvis du vil arbejde igennem flere eksempler!
 Varme artikler
Varme artikler
-
 Nyt materiale opfanger kuldioxidDenne nye porøse koordinationspolymer har propelformede molekylære strukturer, der gør det muligt selektivt at opfange CO2, og effektivt omdanne CO2 til nyttige kulstofmaterialer. Kredit:Mindy Takamiy
Nyt materiale opfanger kuldioxidDenne nye porøse koordinationspolymer har propelformede molekylære strukturer, der gør det muligt selektivt at opfange CO2, og effektivt omdanne CO2 til nyttige kulstofmaterialer. Kredit:Mindy Takamiy -
 Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede
Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede -
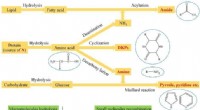 En ny idé til raffinering af bioråolieKredit:Bao et al., Grænser for kemividenskab og ingeniørvidenskab (2022). DOI:10.1007/s11705-021-2126-y Det høje indhold af nitrogenholdige organiske forbindelser (NOCer) i biocrude opnået fra hydr
En ny idé til raffinering af bioråolieKredit:Bao et al., Grænser for kemividenskab og ingeniørvidenskab (2022). DOI:10.1007/s11705-021-2126-y Det høje indhold af nitrogenholdige organiske forbindelser (NOCer) i biocrude opnået fra hydr -
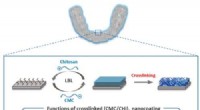 Hjælper tandholdere og aligners med at bekæmpe bakterierKredit:American Chemical Society Klar, plast aligners er vokset i popularitet som alternativer til voluminøse, metal seler. Og når tænderne er rettet, patienter opgraderer til plastikholdere for a
Hjælper tandholdere og aligners med at bekæmpe bakterierKredit:American Chemical Society Klar, plast aligners er vokset i popularitet som alternativer til voluminøse, metal seler. Og når tænderne er rettet, patienter opgraderer til plastikholdere for a
- Navngiv to føderale agenturer, der understøtter astronomisk forskning?
- Hvad er forskellen mellem menneskelig og naturlig luftforurening?
- NASA ser en masse styrke i infrarød visning af kat fire orkanen Walaka
- Hvilke forhold gengiver bakterier i?
- Hvad betyder kæmpe kovalent?
- Hvad er større 1,9 decimetre eller 1900 millimeter?


