Kovalente vs. metalliske bindinger:nøgleforskelle forklaret
Kovalente bindinger
* Formation: Dannes, når to ikke-metalatomer deler elektroner for at opnå en stabil elektronkonfiguration (fyldt ydre skal).
* Elektrondeling: Elektroner deles ligeligt (ikke-polære) eller ulige (polære) mellem atomer.
* Forbindelsesstyrke: Kan være stærk eller svag afhængig af typen af kovalent binding.
* Egenskaber:
* Danner typisk molekyler med lavt smelte- og kogepunkt.
* Dårlige ledere af elektricitet (undtagen grafit).
* Kan være faste stoffer, væsker eller gasser ved stuetemperatur.
* Har ofte lav trækstyrke.
* Eksempler: Vand (H₂O), kuldioxid (CO₂), metan (CH4)
Metallige bindinger
* Formation: Dannet mellem metalatomer, hvor elektroner er delokaliseret (fri til at bevæge sig gennem hele strukturen).
* Elektrondeling: Elektroner er ikke lokaliseret mellem specifikke atomer, men danner et "hav" af elektroner, der deles af alle atomer i den metalliske struktur.
* Forbindelsesstyrke: Generelt stærk på grund af tiltrækningen mellem de positive metalioner og havet af delokaliserede elektroner.
* Egenskaber:
* Fremragende ledere af varme og elektricitet.
* Formbar (kan hamres til plader).
* Duktilt (kan trækkes ind i ledninger).
* Har typisk høje smelte- og kogepunkter.
* Eksempler: Jern (Fe), kobber (Cu), guld (Au)
Her er en tabel, der opsummerer de vigtigste forskelle:
| Funktion | Kovalent binding | Metallic Bond |
|---------------------|---------------|--------------------|
| Atomer involveret | Ikke-metaller | Metaller |
| Elektrondeling | Delt mellem specifikke atomer | Delokaliseret, delt af alle atomer |
| Bindingsstyrke | Variabel | Stærk |
| Ledningsevne | Dårlig | Fremragende |
| Formbarhed | Ikke formbar | Formbar |
| Duktilitet | Ikke duktilt | Duktil |
| Smeltning/kogende Pt | Lav | Høj |
I bund og grund:
* Kovalente bindinger involverer deling af elektroner mellem specifikke atomer, hvilket resulterer i molekyler.
* Metalbindinger involverer et "hav" af delokaliserede elektroner, der deles af alle atomer i strukturen, hvilket fører til metallers unikke egenskaber.
 Varme artikler
Varme artikler
-
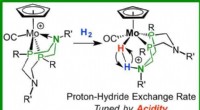 Forskere kontrollerer hastigheden af nedbrydning og fiksering af dihydrogenmolekyleDette molekyle blev genereret in situ ved hydridudvinding fra n-fluorbenzen. Kredit:Pacific Northwest National Laboratory Brint er det mest udbredte grundstof i universet. Dihydrogenmolekylet, med
Forskere kontrollerer hastigheden af nedbrydning og fiksering af dihydrogenmolekyleDette molekyle blev genereret in situ ved hydridudvinding fra n-fluorbenzen. Kredit:Pacific Northwest National Laboratory Brint er det mest udbredte grundstof i universet. Dihydrogenmolekylet, med -
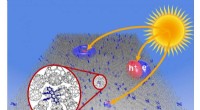 Molekylære vibrationer reducerer den maksimalt opnåelige fotovoltage i organiske solcellerIllustration af generation af ladningspar (excitoner), forløberne til gratis ladningsbærere i det aktive lag af en organisk solcelle. Kredit:Technische Universitaet Dresden Forskere ved TU Dresden
Molekylære vibrationer reducerer den maksimalt opnåelige fotovoltage i organiske solcellerIllustration af generation af ladningspar (excitoner), forløberne til gratis ladningsbærere i det aktive lag af en organisk solcelle. Kredit:Technische Universitaet Dresden Forskere ved TU Dresden -
 Studerer gasmaskefiltre, så folk kan trække vejret lettereKobber, vist her, er en komponent i filtre, der bruges i gasmasker for at beskytte brugere mod giftige kemikalier. Forskere ved Berkeley Lab bruger kraftig røntgenspektroskopi til at studere de moleky
Studerer gasmaskefiltre, så folk kan trække vejret lettereKobber, vist her, er en komponent i filtre, der bruges i gasmasker for at beskytte brugere mod giftige kemikalier. Forskere ved Berkeley Lab bruger kraftig røntgenspektroskopi til at studere de moleky -
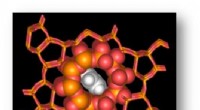 Forskere opdager nye byggesten i katalysatorzeolit -nanoporerUMass Amherst kemikere og materialeforskere har avanceret forståelse af zeolitkatalysatorstruktur og vibrationer for at hjælpe med at føre til nye materialer til ren energi og kulstofopsamling, blandt
Forskere opdager nye byggesten i katalysatorzeolit -nanoporerUMass Amherst kemikere og materialeforskere har avanceret forståelse af zeolitkatalysatorstruktur og vibrationer for at hjælpe med at føre til nye materialer til ren energi og kulstofopsamling, blandt
- Navn på syre, der er til stede i kartoffelchips?
- Hvad bruger videnskabsmand til at repræsentere et system eller et objekt?
- Hvorfor skulle kemikalierne i gødning være opløseligt vand?
- Hvilken erosions agent skabte haven guder?
- Sådan læres diskret matematik
- Hvordan hærmyrernes ikoniske masseangreb udviklede sig


