Forståelse af uopløseligheden af kovalente netværksfaststoffer
1. Stærke kovalente bindinger: Faste stoffer i kovalent netværk holdes sammen af et kontinuerligt netværk af stærke kovalente bindinger. Disse bindinger er meget stærkere end de intermolekylære kræfter (som hydrogenbinding, dipol-dipol eller London-dispersionskræfter), der holder opløsningsmiddelmolekyler sammen, eller som potentielt kan dannes mellem netværksfaststoffet og opløsningsmidlet.
2. Mangel på polaritet: De fleste kovalente netværk er sammensat af ikke-polære atomer. De har intet signifikant dipolmoment og kan ikke danne stærke vekselvirkninger med polære opløsningsmidler.
3. Mangel på "Breakable" websteder: I modsætning til ioniske forbindelser eller molekylære faste stoffer er der ingen let identificerbare steder i et kovalent netværk, hvor opløsningsmiddelmolekyler kan bryde strukturen fra hinanden. At bryde netværket ville kræve at bryde de stærke kovalente bindinger.
4. Høje smeltepunkter: De stærke kovalente bindinger i disse faste stoffer resulterer i ekstremt høje smeltepunkter. De fleste almindelige opløsningsmidler har meget lavere kogepunkter og er ikke i stand til at levere nok energi til at bryde netværket og opløse det faste stof.
Eksempler:
* Diamant: Et kovalent netværk af carbonatomer, det er uopløseligt i alle kendte opløsningsmidler.
* Kvarts (SiO2): Et kovalent netværk af silicium og oxygenatomer, det er i det væsentlige uopløseligt i vand eller andre almindelige opløsningsmidler.
Undtagelser:
Mens kovalente netværk generelt er meget uopløselige, er der nogle undtagelser:
* Nogle kovalente netværk kan opløses i stærkt reaktive opløsningsmidler: For eksempel kan visse kovalente netværk opløses i stærke syrer, baser eller stærkt reaktive oxidationsmidler. Disse opløsningsmidler kan reagere med netværket, bryde bindingerne og opløse det faste stof.
* Der kan forekomme specifikke interaktioner: Selvom opløsningsmidlet ikke er meget reaktivt, kan nogle kovalente netværk udvise begrænset opløselighed i specifikke opløsningsmidler på grund af specifikke interaktioner, såsom svag hydrogenbinding.
Opsummering: Kombinationen af stærke kovalente bindinger, mangel på polaritet og mangel på brydbare steder i kovalente netværksfaststoffer gør dem generelt meget uopløselige i almindelige opløsningsmidler. Selvom der kan være undtagelser, gør disse faktorer at opløse dem i almindelige opløsningsmidler til en meget udfordrende opgave.
Sidste artikelCalcit og saltsyre:den brusende reaktion forklaret
Næste artikelKemilaboratoriers kritiske rolle i forskning og innovation
 Varme artikler
Varme artikler
-
 Verdens ældste insekt inspirerer en ny generation af aerogelerKredit:Newcastle University Et team af internationale videnskabsmænd har skabt en ny form for højeffektive, lavpris isolering baseret på vingerne på en guldsmede. Materialet, kendt som en aerogel
Verdens ældste insekt inspirerer en ny generation af aerogelerKredit:Newcastle University Et team af internationale videnskabsmænd har skabt en ny form for højeffektive, lavpris isolering baseret på vingerne på en guldsmede. Materialet, kendt som en aerogel -
 Omdannelse af kuldioxid til butanol ved hjælp af phosphorrige kobberkatoderForskere fra Gwangju Institute of Science and Technology udviklede en metode til direkte at generere 1-butanol, en alternativ brændstofkilde, fra CO 2 ved brug af kobberphosphidelektroder. Kredit:Gw
Omdannelse af kuldioxid til butanol ved hjælp af phosphorrige kobberkatoderForskere fra Gwangju Institute of Science and Technology udviklede en metode til direkte at generere 1-butanol, en alternativ brændstofkilde, fra CO 2 ved brug af kobberphosphidelektroder. Kredit:Gw -
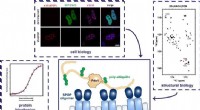 Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr
Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr -
 Metoden undersøger hurtigt atomtynde materialers evne til at producere brintEn teknik udviklet af Rice University og Los Alamos National Laboratory vil give forskere mulighed for hurtigt at undersøge atomtykke materialer for at måle brintproduktion. Rislaboratoriet bruger en
Metoden undersøger hurtigt atomtynde materialers evne til at producere brintEn teknik udviklet af Rice University og Los Alamos National Laboratory vil give forskere mulighed for hurtigt at undersøge atomtykke materialer for at måle brintproduktion. Rislaboratoriet bruger en
- Hvordan så astronomerne himmel, før teleskoper blev opfundet?
- Hvad er formel for øjeblik inerti, du sektionsstråle?
- Udvikling af teknologi til fremstilling af interconnect i mikroskala fra flerlagsgrafen
- Hvad er et nødvendigt produkt af forbrændingsreaktionen?
- Hvordan gendanner du et opløsningsmiddel fra opløsningen?
- Augmented reality-værktøjer til at hjælpe sundhedspersonale med at redde liv i krigszoner, naturk…


