Lineær arrangement af atomer uden enlige par:Forståelse af molekylær geometri
Her er hvorfor:
* Elektronparrepulsion: Elektronparrene i bindingerne frastøder hinanden, og de forsøger at komme så langt fra hinanden som muligt.
* Minimering af frastødning: I et lineært arrangement er de to elektronpar (fra bindingerne) på modsatte sider af det centrale atom, hvilket maksimerer afstanden mellem dem og minimerer frastødning.
Eksempel:
* Kuldioxid (CO2) har et centralt kulstofatom bundet til to oxygenatomer. Der er ingen enlige par på kulstofatomet. Molekylet er lineært.
Sig til, hvis du gerne vil udforske andre molekylære geometrier!
Sidste artikelLithium-atomelektroner:Forståelse af neutralitet og atomstruktur
Næste artikelKlorkogepunkt:Temperatur &faseovergang
 Varme artikler
Varme artikler
-
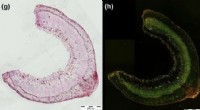 Selvhelbredende materialer inspireret af planterTværsnit af en Linum Drakkar stilk med et 26 dage gammelt sår parallelt med fibrene. Kredit:Cloé Paul-Victor, Albert-Ludwigs-Universitat Freiburg Forskere ved EPFLs Laboratory for Processing of Ad
Selvhelbredende materialer inspireret af planterTværsnit af en Linum Drakkar stilk med et 26 dage gammelt sår parallelt med fibrene. Kredit:Cloé Paul-Victor, Albert-Ludwigs-Universitat Freiburg Forskere ved EPFLs Laboratory for Processing of Ad -
 Hurtige strategier til at huske homonukleære diatomiske molekylerAf Daniel Zimmermann | Opdateret 24. marts 2022 I kemi består et diatomisk molekyle af kun to atomer. Når begge atomer tilhører det samme grundstof og deler identisk nuklear sammensætning – samme ant
Hurtige strategier til at huske homonukleære diatomiske molekylerAf Daniel Zimmermann | Opdateret 24. marts 2022 I kemi består et diatomisk molekyle af kun to atomer. Når begge atomer tilhører det samme grundstof og deler identisk nuklear sammensætning – samme ant -
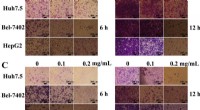 Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand
Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand -
 Enkel metode til keramisk-baserede fleksible elektrolytplader til lithiummetalbatterierI den nærmeste fremtid, lithiummetalbatterier med en fleksibel LLZO elektrolytplade kan bruges i avancerede elektriske køretøjer (EVer). Kredit:Tokyo Metropolitan University 1000°C) processer. Den
Enkel metode til keramisk-baserede fleksible elektrolytplader til lithiummetalbatterierI den nærmeste fremtid, lithiummetalbatterier med en fleksibel LLZO elektrolytplade kan bruges i avancerede elektriske køretøjer (EVer). Kredit:Tokyo Metropolitan University 1000°C) processer. Den
- Hvordan dannes bioklastisk bjergart?
- Rekordlav 2016 havis i Antarktis på grund af perfekt tropisk storm, polære forhold
- Ny algoritme udvider brugen af avanceret kamera til biologisk mikroskopi
- Hvordan skabes solenergi?
- Astronomer finder superhobe af galakser nær Mælkevejen
- Hvem var en vigtig videnskabsmand inden for opdagelser af rummet?


