Fluor- og natriumbromidreaktion:Forståelse af forskydningsmekanismen
Her er hvorfor:
* Fluor er mere reaktivt end brom. Dette skyldes dens højere elektronegativitet og mindre atomstørrelse, hvilket gør det til et stærkere oxidationsmiddel.
* Fluor fortrænger brom fra natriumbromid. Det mere reaktive fluor vil reagere med natrium og danne natriumfluorid (NaF), mens bromet fortrænges og danner elementært brom (Br₂).
Den afbalancerede kemiske ligning er:
F₂ (g) + 2NaBr (aq) → 2NaF (aq) + Br₂ (l)
Nøglepunkter:
* Denne reaktion er meget eksoterm, hvilket betyder, at den frigiver meget varme.
* Reaktionen er et godt eksempel på halogenreaktivitetstrenden, hvor halogenernes reaktivitet falder ned i gruppen (fra fluor til jod).
* Reaktionen er også et eksempel på en redoxreaktion, hvor fluor reduceres og brom oxideres.
Sidste artikelSvovlsyre og stensaltreaktion:farer og produkter
Næste artikelMetalrenhedstestning:Hvorfor et termometer ikke er nok
 Varme artikler
Varme artikler
-
 Skaber bomuld, der er brandsikkert og behageligtOmkostningseffektiv:Sabyasachi Gaan bruger damp fra en kommerciel trykkoger til at flammehæmme prøver af bomuldsstof. Kredit:Empa Avancerede flammehæmmende bomuldstekstiler lider under frigivelse
Skaber bomuld, der er brandsikkert og behageligtOmkostningseffektiv:Sabyasachi Gaan bruger damp fra en kommerciel trykkoger til at flammehæmme prøver af bomuldsstof. Kredit:Empa Avancerede flammehæmmende bomuldstekstiler lider under frigivelse -
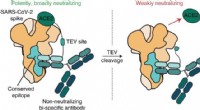 Molekylær makeover gør wimpy antistof til en SARS-CoV-2 tacklerGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01140-1 Ligesom Roadrunner, der overliste Wile E. Coyote, bliver SARS-CoV-2 (den infektiøse virus, der er ansvarlig f
Molekylær makeover gør wimpy antistof til en SARS-CoV-2 tacklerGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01140-1 Ligesom Roadrunner, der overliste Wile E. Coyote, bliver SARS-CoV-2 (den infektiøse virus, der er ansvarlig f -
 Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit
Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit -
 Inde i brændselscellen:Imaging metode lover industriel indsigtHydrogenholdige stoffer er vigtige for mange industrier, men forskere har kæmpet for at få detaljerede billeder for at forstå elementets adfærd. I gennemgang af videnskabelige instrumenter, forskere d
Inde i brændselscellen:Imaging metode lover industriel indsigtHydrogenholdige stoffer er vigtige for mange industrier, men forskere har kæmpet for at få detaljerede billeder for at forstå elementets adfærd. I gennemgang af videnskabelige instrumenter, forskere d


