Forståelse af ikke-polære kovalente bindinger:Equal Electron Sharing
Her er hvorfor:
* Polaritet: Udtrykket "polær" henviser til fordelingen af elektrisk ladning i et molekyle. I en ikke-polær kovalent binding deles elektronerne ligeligt, hvilket betyder, at der ikke er nogen signifikant forskel i ladningen mellem de to atomer.
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner. Når to atomer har lignende elektronegativitetsværdier, deler de elektroner ligeligt, hvilket resulterer i en ikke-polær kovalent binding.
Eksempler på ikke-polære kovalente bindinger:
* H₂ (brintgas): Begge brintatomer har den samme elektronegativitet, så de deler elektronerne ligeligt.
* O₂ (iltgas): Begge iltatomer har samme elektronegativitet, så de deler elektronerne ligeligt.
* Cl₂ (klorgas): Begge kloratomer har samme elektronegativitet, så de deler elektronerne ligeligt.
Nøgleafhentning: I ikke-polære kovalente bindinger deles elektronerne ligeligt mellem atomerne, hvilket resulterer i en afbalanceret fordeling af ladningen.
 Varme artikler
Varme artikler
-
 Bredere applikationer til udkogning af en ægmaskineProfessor Colin Raston, professor i ren teknologi, College of Science and Engineering. Kredit:Flinders University Bredere rene kemi -applikationer af den ekstraordinære Vortex Fluidic Device - opf
Bredere applikationer til udkogning af en ægmaskineProfessor Colin Raston, professor i ren teknologi, College of Science and Engineering. Kredit:Flinders University Bredere rene kemi -applikationer af den ekstraordinære Vortex Fluidic Device - opf -
 En ny forståelse af proteinbevægelseEt team af ingeniører har vist, at overfladediffusion i proteintransport til ionbytterperler afhænger af adsorptionsaffinitet - et mål for tiltrækning mellem de to materialer. Kredit:University of Del
En ny forståelse af proteinbevægelseEt team af ingeniører har vist, at overfladediffusion i proteintransport til ionbytterperler afhænger af adsorptionsaffinitet - et mål for tiltrækning mellem de to materialer. Kredit:University of Del -
 Elektricitetsdrevne undersøiske reaktioner kan have været vigtige for livets opståenForskningsgruppen har foreslået en effektiv mekanisme til at udnytte den kemiske energi, der genereres af varme hydrotermiske væsker, der strømmer ud af hydrotermiske ventilationsåbninger på Jordens t
Elektricitetsdrevne undersøiske reaktioner kan have været vigtige for livets opståenForskningsgruppen har foreslået en effektiv mekanisme til at udnytte den kemiske energi, der genereres af varme hydrotermiske væsker, der strømmer ud af hydrotermiske ventilationsåbninger på Jordens t -
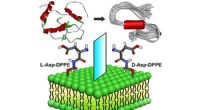 Nye fund kaster lys over udviklingen af liposom-baserede hæmmereMolekylær chiralitet medieret amyloiddannelse på phospholipidoverflader. Kredit:WANG Xue Alzheimers sygdom (AD) er en af de største globale folkesundhedsudfordringer. Imidlertid, patogenesen af
Nye fund kaster lys over udviklingen af liposom-baserede hæmmereMolekylær chiralitet medieret amyloiddannelse på phospholipidoverflader. Kredit:WANG Xue Alzheimers sygdom (AD) er en af de største globale folkesundhedsudfordringer. Imidlertid, patogenesen af
- SimRadar:En polarimetrisk radarsimulator i tidsserier til undersøgelser af tornadisk affald
- Forskere undersøger befolkningsstørrelse, tæthed i stigningen af centraliseret magt i antikken
- Hvilken genstand repræsenterer en simpel maskine batteri tang tændstik eller stearinlys?
- Forskning viser, hvorfor meteroider eksploderer, før de når Jorden
- Et objekt, der rejser 250 m i 25s, har hvilken hastighed?
- Reagerer vand på dets miljø?


