Syre-base reaktioner:Forståelse af oxid + vand reaktioner
* Syre: Syrer donerer hydrogenioner (H+) i opløsning.
* Ikke-metaloxid: Ikke-metaloxider er sure oxider, hvilket betyder, at de reagerer med vand og danner syrer.
* Vand: Vand fungerer som et opløsningsmiddel, der tillader syren og ikke-metaloxidet at reagere.
Sådan virker det:
1. Ikke-metaloxid reagerer med vand: Ikke-metaloxidet opløses i vand og danner en syre. For eksempel:
* CO₂ (kuldioxid) + H₂O (vand) → H₂CO₃ (kulsyre)
2. Syre reagerer med syren dannet i trin 1: Den oprindelige syre neutraliserer den syre, der dannes af ikke-metaloxidet. Dette involverer hydrogenionerne (H+) fra den oprindelige syre, der reagerer med anionerne (negative ioner) fra syren dannet af ikke-metaloxidet.
* HCl (saltsyre) + H₂CO₃ (kulsyre) → H₂O (vand) + CO₂ (kuldioxid) + 2Cl⁻ (chloridioner)
Samlet set kan reaktionen opsummeres som:
Syre + Ikke-metaloxid + Vand → Salt + Vand
Eksempel:
* HCl (saltsyre) + SO₂ (svovldioxid) + H2O (vand) → H₂SO₄ (svovlsyre) + H2O (vand)
Her reagerer svovldioxid (SO₂) med vand og danner svovlsyrling (H₂SO3). Derefter reagerer saltsyre (HCl) med svovlsyrling og danner vand, svovlsyre (H2SO4) og chloridioner (Cl-).
Vigtige bemærkninger:
* Ikke alle ikke-metaloxider reagerer med vand. Nogle, som kulilte (CO), er relativt ureaktive.
* De specifikke produkter vil afhænge af identiteten af syren og ikke-metaloxidet.
Sig til, hvis du vil udforske specifikke eksempler eller har yderligere spørgsmål!
Sidste artikelOpløst stof Forklaret:Forståelse af opløsning i vand
Næste artikelBeregning af mol af oxidioner:en trin-for-trin guide
 Varme artikler
Varme artikler
-
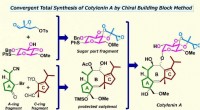 Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s
Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s -
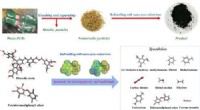 Mod sikrere bortskaffelse af printkortKredit:American Chemical Society Printplader er vitale komponenter i moderne elektronik. Imidlertid, når de har tjent deres formål, de bliver ofte brændt eller begravet på lossepladser, forurener
Mod sikrere bortskaffelse af printkortKredit:American Chemical Society Printplader er vitale komponenter i moderne elektronik. Imidlertid, når de har tjent deres formål, de bliver ofte brændt eller begravet på lossepladser, forurener -
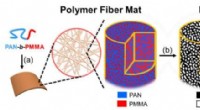 Porøs kulfiberforskning et skridt nærmere brug i bilindustrienSyntese af porøse kulfibre og belastning af MnO2. (a) En diblokcopolymer af polyacrylonitril-blok-polymethylmethacrylat (PAN-b-PMMA) spindes ind i en polymerfibermåtte. I den forstørrede udsigt, blokc
Porøs kulfiberforskning et skridt nærmere brug i bilindustrienSyntese af porøse kulfibre og belastning af MnO2. (a) En diblokcopolymer af polyacrylonitril-blok-polymethylmethacrylat (PAN-b-PMMA) spindes ind i en polymerfibermåtte. I den forstørrede udsigt, blokc -
 Beregning af et molekyles masse i gram:en praktisk vejledningAf Chris Deziel Opdateret 24. marts 2022 alice-photo/iStock/GettyImages For at bestemme en forbindelses molekylmasse skal du kende dens molekylære formel og atommassen af hvert element. Atommasser
Beregning af et molekyles masse i gram:en praktisk vejledningAf Chris Deziel Opdateret 24. marts 2022 alice-photo/iStock/GettyImages For at bestemme en forbindelses molekylmasse skal du kende dens molekylære formel og atommassen af hvert element. Atommasser
- Hvad er den afbalancerede ligning til at repræsentere nedbrydning af bly IV -oxid?
- Hvor lang tid tager det en impuls at rejse 10 meter?
- Hvilket grundstof er der i kulkalksten og petroleum?
- Hvad producerer fotosyntesen mad til?
- Hvad skal Magma gøre for en rockform?
- Hvorfor har forskellige elektriske enheder wattager?


