Beregning af et molekyles masse i gram:en praktisk vejledning
Af Chris Deziel Opdateret 24. marts 2022
alice-photo/iStock/GettyImages
For at bestemme en forbindelses molekylmasse skal du kende dens molekylære formel og atommassen af hvert element. Atommasser, udtrykt i atommasseenheder (amu), er opført under hvert elements symbol i det periodiske system. Per definition er atommassen af et grundstof lig med massen af et mol af dette grundstof i gram. En muldvarp indeholder Avogadros tal (6,02 × 10 23 ) af atomer eller molekyler.
TL;DR (for lang; læste ikke)
Tilføj atommasserne af alle atomer i et molekyles formel for at opnå massen af et mol i gram.
Den molekylære formel
Atomer binder sig efter fordelingen af valenselektroner. Ioniske forbindelser, såsom natriumchlorid (NaCl), består af et atom af hver af to forskellige grundstoffer. Kovalente gasser som brint (H₂) og oxygen (O₂) indeholder to identiske atomer. Komplekse molekyler, især organiske forbindelser, kan indeholde snesevis af atomer; for eksempel indeholder glucose (C₆H₁2O6) 24 atomer.
Uanset størrelse er beregningsmetoden identisk:slå hvert grundstofs atommasse op, gange med dets antal i formlen, og summer derefter alle bidrag. Resultatet er molmassen i gram.
Slå op på atommassetal
Grundstoffer er arrangeret i det periodiske system ved at øge atomnummeret, hvilket er lig med antallet af protoner i kernen. Brint, med én proton, er først; oxygen, med otte protoner, er ottende. Atomnummer adskiller sig fra atommasse, fordi neutroner også bidrager til massen. Elektroner er ubetydelige i masse. Atommassen – summen af protoner og neutroner – er angivet under hvert elements symbol.
Afrund til nærmeste heltal: Atommasseværdier inkluderer ofte decimaler på grund af naturlig isotopvariation. For de fleste praktiske formål, afrund til nærmeste hele tal. For eksempel er oxygens listede masse 15.999; afrunding giver 16, hvilket betyder, at et mol ilt vejer 16g.
Eksempel
Hvad er molekylmassen af glucose i gram?
Glucoses formel er C₆H₁₂O6. Fra det periodiske system er kulstof (C) =12 amu, hydrogen (H) =1 amu, oxygen (O) =16 amu. Den molære masse er lig med (6×12)+(12×1)+(6×16)=180g/mol. Således har et mol glucose en masse på 180 g. For at finde massen af flere mol skal du gange 180g med antallet af mol.
 Varme artikler
Varme artikler
-
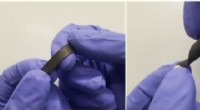 Den følsomme belastningssensor, der kan registrere vægten af en fjerStrækker og vrider de ultrafølsomme belastningssensorer. Kredit:University of Sussex Fysikere har skabt den mest følsomme belastningssensor, der nogensinde er lavet, i stand til at registrere en f
Den følsomme belastningssensor, der kan registrere vægten af en fjerStrækker og vrider de ultrafølsomme belastningssensorer. Kredit:University of Sussex Fysikere har skabt den mest følsomme belastningssensor, der nogensinde er lavet, i stand til at registrere en f -
 Fremtiden for plastik – genbruge det dårlige og opmuntre det godePlastforurening:kasserede plastikposer er en fare for livet i havet. Kredit:Richard Whitcombe/Shutterstock, CC BY-ND Plast har fået et dårligt navn, hovedsagelig af to grunde:de fleste er lavet af
Fremtiden for plastik – genbruge det dårlige og opmuntre det godePlastforurening:kasserede plastikposer er en fare for livet i havet. Kredit:Richard Whitcombe/Shutterstock, CC BY-ND Plast har fået et dårligt navn, hovedsagelig af to grunde:de fleste er lavet af -
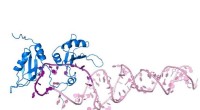 Ny indsigt i modning af miRNA'erForfatterne var i stand til at vise nøjagtigt, hvordan et specifikt RNA-bindende protein (blåt) genkender pri-miR-18a (pink) og ændrer dets struktur på en sådan måde, at det udvikler sig til modent mi
Ny indsigt i modning af miRNA'erForfatterne var i stand til at vise nøjagtigt, hvordan et specifikt RNA-bindende protein (blåt) genkender pri-miR-18a (pink) og ændrer dets struktur på en sådan måde, at det udvikler sig til modent mi -
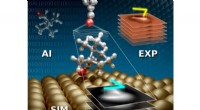 Ny tværfaglig tilgang til at identificere komplekse molekylære adsorbaterKunstig intelligens (AI) forbedret ab-initio struktursøgning kombineres med atomic force microscopy simulations (SIM) og eksperimenter (EXP) for at detektere konfigurationer af omfangsrige 3D-adsorbat
Ny tværfaglig tilgang til at identificere komplekse molekylære adsorbaterKunstig intelligens (AI) forbedret ab-initio struktursøgning kombineres med atomic force microscopy simulations (SIM) og eksperimenter (EXP) for at detektere konfigurationer af omfangsrige 3D-adsorbat
- Hvilken type protist ligner den mest svamp?
- Udenlandske virksomheder i Kina forbereder sig på VPN-krak
- Hyperspektral imager efterlader en arv af bidrag til kystforskning
- Astronomer afslører kosmiske udbrud i nærliggende galakser
- Hvorfor er transmissionspositronmikroskop og akustisk vigtig for at forstå, hvordan levende celler …
- Virus-relaterede svindelordninger koster amerikanske forbrugere næsten 5 mio. USD


