Forståelse af kovalente bindinger:Enkelt-, dobbelt- og tredobbeltbindinger forklaret
Kovalente bindinger:Deling er omsorgsfuld
Kovalente bindinger opstår, når to atomer deler elektroner for at opnå en stabil elektronkonfiguration (normalt en fuld ydre skal).
1. Enkelt kovalent binding
* Deling: To atomer deler et par elektroner (to elektroner i alt).
* Repræsentation: En enkelt linje trukket mellem atomernes symboler, fx H-H (brintmolekyle).
* Eksempel: Bindingen i et brintmolekyle (H₂) eller bindingerne i et methanmolekyle (CH4).
2. Dobbelt kovalent binding
* Deling: To atomer deler to par elektroner (fire elektroner i alt).
* Repræsentation: To streger trukket mellem atomernes symboler, fx O=O (iltmolekyle).
* Eksempel: Bindingen i et iltmolekyle (O₂), eller bindingerne i et carbondioxidmolekyle (CO₂).
3. Tredobbelt kovalent binding
* Deling: To atomer deler tre par elektroner (seks elektroner i alt).
* Repræsentation: Tre linjer tegnet mellem atomernes symboler, f.eks. N≡N (nitrogenmolekyle).
* Eksempel: Bindingen i et nitrogenmolekyle (N2), eller bindingerne i et hydrogencyanidmolekyle (HCN).
Nøglepunkter at huske:
* Styrke: Generelt er tredobbeltbindinger de stærkeste, efterfulgt af dobbeltbindinger og derefter enkeltbindinger. Dette skyldes, at flere elektroner deles, hvilket fører til en større tiltrækningskraft mellem atomerne.
* Forbindelseslængde: Tredobbeltbindinger er de korteste, efterfulgt af dobbeltbindinger og derefter enkeltbindinger. Den øgede elektrondeling trækker atomerne tættere sammen.
* Bindningsvinkel: Antallet af bindinger kan påvirke formen af et molekyle. For eksempel er dobbeltbindinger mere stive end enkeltbindinger, hvilket fører til ændringer i bindingsvinkler.
Visuelt eksempel:
Forestil dig et par hænder, der holder en bold sammen. Dette er som en enkelt binding. Forestil dig nu, at begge hænder holder to bolde hver. Det er en dobbeltbinding. Forestil dig endelig, at hver hånd holder tre bolde. Det er et tredobbelt bånd!
Sig til, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
 Forskere opdager ny strategi for udvikling af menneskeintegreret elektronikKredit:Unsplash/CC0 Public Domain Polymerhalvledere - materialer, der er blevet gjort bløde og elastiske, men stadig i stand til at lede elektricitet - lover fremtidig elektronik, der kan integrer
Forskere opdager ny strategi for udvikling af menneskeintegreret elektronikKredit:Unsplash/CC0 Public Domain Polymerhalvledere - materialer, der er blevet gjort bløde og elastiske, men stadig i stand til at lede elektricitet - lover fremtidig elektronik, der kan integrer -
 Innovative DNA -genopretningsteknikker kan hjælpe ofre med at fange voldtægtsmænd i KenyaEn måde at tackle denne voldelige kriminalitet på er gennem DNA -profilering. Kredit:vitstudio/Shutterstock En kæmpe global sundhedsudfordring er fysisk og seksuel vold mod kvinder og piger, påvir
Innovative DNA -genopretningsteknikker kan hjælpe ofre med at fange voldtægtsmænd i KenyaEn måde at tackle denne voldelige kriminalitet på er gennem DNA -profilering. Kredit:vitstudio/Shutterstock En kæmpe global sundhedsudfordring er fysisk og seksuel vold mod kvinder og piger, påvir -
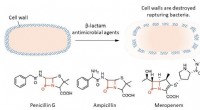 En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende
En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende -
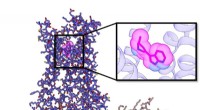 Forskere skaber ikke-psykedeliske forbindelser med samme antidepressive effektRepræsentation af serotonin 2A-receptoren (5HT2AR) signalerende proteinkompleks bundet til den nye forbindelse R-69 (i undergruppe, magenta). Kredit:Roth Lab, UNC School of Medicine Selvom det er u
Forskere skaber ikke-psykedeliske forbindelser med samme antidepressive effektRepræsentation af serotonin 2A-receptoren (5HT2AR) signalerende proteinkompleks bundet til den nye forbindelse R-69 (i undergruppe, magenta). Kredit:Roth Lab, UNC School of Medicine Selvom det er u
- Hvor stammer stjernerne?
- Hvad er det generelle forholdsnummer på måner, som en planet har sammenlignet med dens masse?
- Sådan gør du en elektromagnet stærkere:4 gennemprøvede teknikker
- Hvilken procentdel af den energi, der bruges i verden, er uran?
- Sådan beregnes eksperimentel værdi
- Lava fra La Palma -udbrud når endelig Atlanterhavet


