Sølvnitrat- og karbonatreaktion:En kemisk udfældningsforklaring
Her er den afbalancerede kemiske ligning for reaktionen:
2AgNO3(vandig) + Na2CO3(vandig) → Ag2CO3(s) + 2NaNO3(vandig)
Lad os nedbryde, hvad der sker:
* Sølvioner (Ag⁺) fra sølvnitratopløsningen reagerer med carbonationer (CO₃²⁻) fra carbonatopløsningen.
* Sølvcarbonat (Ag₂CO₃) er uopløseligt i vand, hvilket betyder, at det ikke opløses og danner et fast bundfald.
* De resterende ioner, natriumioner (Na⁺) og nitrationer (NO3⁻) , forblive opløst i opløsning som natriumnitrat (NaNO₃) .
Nøgleobservationer:
* Danning af et hvidt bundfald: Dette er en klar indikation af reaktionen.
* Bundfaldet er uopløseligt: Det vil sætte sig i bunden af beholderen.
Denne reaktion er et klassisk eksempel på en dobbeltforskydningsreaktion, hvor de positive og negative ioner af to reaktanter skifter plads, hvilket fører til dannelsen af nye forbindelser.
 Varme artikler
Varme artikler
-
 Hurtig test til diagnosticering af astmaDet holografiske mikroskop muliggør automatisk, tredimensionel sporing af immunceller i realtid. Kredit:Fraunhofer-Gesellschaft Astma er en af de mest almindelige luftvejssygdomme i verden, påvi
Hurtig test til diagnosticering af astmaDet holografiske mikroskop muliggør automatisk, tredimensionel sporing af immunceller i realtid. Kredit:Fraunhofer-Gesellschaft Astma er en af de mest almindelige luftvejssygdomme i verden, påvi -
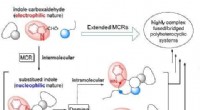 Nye multikomponentreaktionsgrænserEksperterne skaber et hovedprincip, hvormed polaritetsændringen af en reaktiv i en multikomponentproces afkæder domino -reaktioner. Kredit:Angewandte Chemie International Edition Syntesen af k
Nye multikomponentreaktionsgrænserEksperterne skaber et hovedprincip, hvormed polaritetsændringen af en reaktiv i en multikomponentproces afkæder domino -reaktioner. Kredit:Angewandte Chemie International Edition Syntesen af k -
 Forskere udvikler en biologisk nedbrydelig legering til knogleimplantater til frakturer, osteoporose…Lederen af Hybrid Nanostructured Materials Laboratory ved NUST MISIS Alexander Komissarov. Kredit:Maria Brodskaya/NUST MISIS Materialeforskere fra NUST MISIS og University of Western Australia h
Forskere udvikler en biologisk nedbrydelig legering til knogleimplantater til frakturer, osteoporose…Lederen af Hybrid Nanostructured Materials Laboratory ved NUST MISIS Alexander Komissarov. Kredit:Maria Brodskaya/NUST MISIS Materialeforskere fra NUST MISIS og University of Western Australia h -
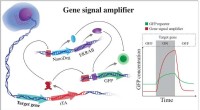 Stærke signaler viser, hvordan proteiner kommer og gårGensignalforstærkeren udviklet af bioscientists ved Rice University udmærker sig ved at detektere ekspressionen af målgener og kan også bruges til at detektere potentielt ethvert cellulært gen. Fors
Stærke signaler viser, hvordan proteiner kommer og gårGensignalforstærkeren udviklet af bioscientists ved Rice University udmærker sig ved at detektere ekspressionen af målgener og kan også bruges til at detektere potentielt ethvert cellulært gen. Fors
- Papirbaseret enhed giver lavt strømforbrug, langsigtet metode til at analysere sved
- Hvordan flytter energi fra det ene niveau til det næste?
- Hvad er molariteten af Carborane Superacid?
- Blinker lyset af jævnt ru overflader?
- DNA fra inka-dreng, der blev ofret for 500 år siden, viser, hvordan mennesker spredte sig til Sydam…
- Hvor lang tid skinner solen på en klar dag?


