Sølvnitrat og jernreaktion:en detaljeret forklaring
Reaktion:
* Sølvnitrat (AgNO₃) , en farveløs opløsning, reagerer med jern (Fe) , et solidt metal.
* Jo mere reaktivt jern fortrænger jo mindre reaktivt sølv fra sølvnitratopløsningen.
* Jern(II)nitrat (Fe(NO₃)₂) , en grønlig opløsning, dannes.
* Sølv (Ag) , et fast metal, afsættes ud af opløsningen som et gråligt-hvidt bundfald.
Ligning:
2 AgNO3(aq) + Fe(s) → Fe(NO3)₂(aq) + 2 Ag(s)
Observationer:
* Du vil observere et gråligt-hvidt bundfald, der dannes på overfladen af jernmetallet.
* Opløsningen bliver fra farveløs til grønlig.
* Jernmetallet vil begynde at opløses.
Forklaring:
Denne reaktion opstår, fordi jern er mere reaktivt end sølv på reaktivitetsrækken af metaller. Det betyder, at jern har en stærkere tendens til at miste elektroner og danne positive ioner. I reaktionen mister jernatomer elektroner for at danne Fe²⁺-ioner, mens sølvioner (Ag⁺) i opløsningen får elektroner og bliver til sølvatomer.
Bemærk:
* Reaktionen kan fremskyndes ved at opvarme opløsningen eller ved at bruge en mere koncentreret opløsning af sølvnitrat.
* Reaktionen kan bruges til at fremstille sølvmetal fra sølvnitratopløsninger.
* Denne reaktion er også et godt eksempel på en redoxreaktion, hvor elektroner overføres fra jern til sølv.
 Varme artikler
Varme artikler
-
 Forskere bruger kooperativ handling af et ligand-counterion-system til bæredygtig etherproduktionForskere bruger samvirkende handling af et ligand-modion-system til bæredygtig etherproduktion, der er nødvendig for farmaceutiske anvendelser. Kredit:Ritsumeikan University Den fortsatte udvikling
Forskere bruger kooperativ handling af et ligand-counterion-system til bæredygtig etherproduktionForskere bruger samvirkende handling af et ligand-modion-system til bæredygtig etherproduktion, der er nødvendig for farmaceutiske anvendelser. Kredit:Ritsumeikan University Den fortsatte udvikling -
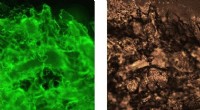 Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot
Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot -
 Methanolsyntese:Indblik i strukturen af en gådefuld katalysatorCarbon-2-Chem-projektet sigter mod at anvende udstødningsgasser fra industrien på en gennemførlig måde. Kredit:RUB, Marquard Metanol er en af de vigtigste basiskemikalier, der bruges, for eksemp
Methanolsyntese:Indblik i strukturen af en gådefuld katalysatorCarbon-2-Chem-projektet sigter mod at anvende udstødningsgasser fra industrien på en gennemførlig måde. Kredit:RUB, Marquard Metanol er en af de vigtigste basiskemikalier, der bruges, for eksemp -
 Ny undersøgelse afslører, at protonhydreringsstrukturer er asymmetriskeKredit:CC0 Public Domain Hvordan vand solvaterer og transporterer protoner er et grundlæggende spørgsmål, som både kemikere og biologer står over for, og det er afgørende for vores forståelse af p
Ny undersøgelse afslører, at protonhydreringsstrukturer er asymmetriskeKredit:CC0 Public Domain Hvordan vand solvaterer og transporterer protoner er et grundlæggende spørgsmål, som både kemikere og biologer står over for, og det er afgørende for vores forståelse af p
- Eksperimentel evolution afslører, hvordan bakterier får lægemiddelresistens
- Med en umættelig efterspørgsel efter datacentre, nogle er bekymrede Illinois kan ikke følge med
- Hvordan falske videnskabelige websteder kaprer vores tillid til eksperter for at misinformere og for…
- Hvordan afgør forskere, om der er sket en atomsprængning?
- Hvor har en bold den største potentielle energi?
- Hemmeligheden ved at måle en antineutrinos energi


