Forudsigelse af redoxreaktioner:Sølv- og kobberion-interaktioner
Forstå begreberne
* Redox-reaktioner: Indebærer overførsel af elektroner. Oxidation er tab af elektroner, og reduktion er forstærkning af elektroner.
* Aktivitetsserie: En liste over metaller arrangeret i rækkefølge efter deres reaktivitet, med de mest reaktive øverst. Dette hjælper med at forudsige, hvilket metal der vil blive oxideret, og hvilket metal der vil blive reduceret.
Anvendelse af koncepterne
1. Aktivitetsserie: Sølv (Ag) er mindre reaktivt end kobber (Cu). Dette betyder, at kobber er mere tilbøjelige til at miste elektroner (oxidere), og sølv er mere tilbøjelige til at få elektroner (reducere).
2. Mulige reaktioner: Der er to mulige reaktioner:
* Reaktion 1: Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
* Kobber (Cu) oxideres til Cu²⁺.
* Sølvioner (Ag⁺) reduceres til sølvmetal (Ag).
* Reaktion 2: Ag(s) + Cu²⁺(aq) → Ingen reaktion
* Denne reaktion er usandsynlig, fordi sølv er mindre reaktivt end kobber.
Konklusion
Den mest sandsynlige redoxreaktion er:
Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
Denne reaktion vil opstå, fordi kobber er mere reaktivt end sølv og derfor er mere tilbøjelige til at donere elektroner til sølvionerne.
 Varme artikler
Varme artikler
-
 Forskere opdager materiale, der er ideelt til smarte solcellevinduerFremskyndede video af materiale, der skifter fra lav-T- til høj-T-fase. Kredit:Berkeley Lab Smarte vinduer, der er gennemsigtige, når det er mørkt eller køligt, men som automatisk bliver mørkere,
Forskere opdager materiale, der er ideelt til smarte solcellevinduerFremskyndede video af materiale, der skifter fra lav-T- til høj-T-fase. Kredit:Berkeley Lab Smarte vinduer, der er gennemsigtige, når det er mørkt eller køligt, men som automatisk bliver mørkere, -
 Comb alkometer er nu tusind gange mere følsom over for sygdomsbiomarkørerKandidatstuderende Qizhong Liang justerer JILAs frekvenskam-alkometer, som identificerer molekyler forbundet med sygdom baseret på farver og mængder af lys absorberet inde i røret (til venstre), der i
Comb alkometer er nu tusind gange mere følsom over for sygdomsbiomarkørerKandidatstuderende Qizhong Liang justerer JILAs frekvenskam-alkometer, som identificerer molekyler forbundet med sygdom baseret på farver og mængder af lys absorberet inde i røret (til venstre), der i -
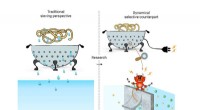 Aktiv sigtning kunne forbedre dialyse- og vandrensningsfiltreFor at adskille molekyler bruges normalt et colander-filter (venstre side). En ny type filter, hvor hullerne i sien kan aktiveres udforskes. (Højre side) Takket være en ekstern strømindgang, hullerne
Aktiv sigtning kunne forbedre dialyse- og vandrensningsfiltreFor at adskille molekyler bruges normalt et colander-filter (venstre side). En ny type filter, hvor hullerne i sien kan aktiveres udforskes. (Højre side) Takket være en ekstern strømindgang, hullerne -
 Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol
Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol
- Forskere er ved at opdage måder at eliminere PFAS på, men dette voksende globale sundhedsproblem f…
- Vejen bliver hårdere for elbil -innovatøren Tesla
- Hvor mange gange ville Jorden passe ind i Antares?
- Styrker immunterapi mod kræft med nanopartikler
- Hvad betyder energiproduktion?
- Hvorfor er benzinheterogen eller homogen?


