Forudsigelse af redoxreaktioner:Sølv og kobber i ioniske løsninger
Forstå redoxreaktioner
* Oxidation: Tab af elektroner
* Reduktion: Forstærkning af elektroner
* Redox-reaktion: En reaktion, der involverer både oxidation og reduktion.
Aktivitetsserie
Metallers reaktivitet er opsummeret i aktivitetsrækken. Metaller højere på serien er mere tilbøjelige til at miste elektroner (oxidere) og forskyde metaller lavere i serien.
* Flere aktive metaller: Højere i aktivitetsrækken.
* Mindre aktive metaller: Lavere i aktivitetsserien.
Nøglespillerne
* Sølv (Ag): Mindre aktiv end kobber.
* Kobber (Cu): Mere aktiv end sølv.
Den sandsynlige reaktion
Da kobber er mere aktivt end sølv, vil det blive oxideret (taber elektroner) og fortrænge sølv fra en opløsning, der indeholder sølvioner:
Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
Forklaring:
* Kobber (Cu) er oxideret: Den mister to elektroner og bliver til en kobber(II)-ion (Cu²⁺).
* Sølvioner (Ag⁺) reduceres: De får elektroner og bliver til fast sølv (Ag).
Vigtig bemærkning: De specifikke ioner, der er til stede i opløsningen, vil afgøre, om denne reaktion faktisk er mulig. Hvis opløsningen f.eks. kun indeholder kobberioner, ville reaktionen ikke forekomme.
 Varme artikler
Varme artikler
-
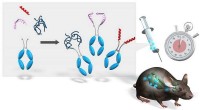 Forskere skaber effektiv semisyntese af biofarmaceutiske-Fc-konjugaterBiopharmaceutic-Fc-konjugat syntetiseret ved vores metode havde en lang halveringstid inde i kroppen. Kredit:University of Electro Communications Biofarmaceutik bestående af mellemmolekyler, for e
Forskere skaber effektiv semisyntese af biofarmaceutiske-Fc-konjugaterBiopharmaceutic-Fc-konjugat syntetiseret ved vores metode havde en lang halveringstid inde i kroppen. Kredit:University of Electro Communications Biofarmaceutik bestående af mellemmolekyler, for e -
 Kunstig cyanobakteriel biofilm kan opretholde produktionen af grøn ethylen i over en månedEt billede af cyanobakterier, Tolypothrix. Kredit:Wikipedia / CC BY-SA 3.0 Vor tids store globale udfordringer, herunder klimaforandringer, energisikkerhed og knaphed på naturressourcer, fremme en
Kunstig cyanobakteriel biofilm kan opretholde produktionen af grøn ethylen i over en månedEt billede af cyanobakterier, Tolypothrix. Kredit:Wikipedia / CC BY-SA 3.0 Vor tids store globale udfordringer, herunder klimaforandringer, energisikkerhed og knaphed på naturressourcer, fremme en -
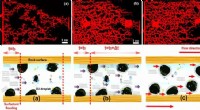 En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati -
 Ikke at tage fejl af australsk bøf – fødevareagility-projektet tackler fødevaresvindelKredit:CC0 Public Domain Tre tons australsk oksekød pakket i Casino NSW og på vej til Kina bliver sporet og verificeret ved hjælp af blockchain og Internet of Things teknologier. Forsendelsen er
Ikke at tage fejl af australsk bøf – fødevareagility-projektet tackler fødevaresvindelKredit:CC0 Public Domain Tre tons australsk oksekød pakket i Casino NSW og på vej til Kina bliver sporet og verificeret ved hjælp af blockchain og Internet of Things teknologier. Forsendelsen er
- Sådan certificeres en kvantecomputer
- Hvorfor udsendt gammastråling i kernen?
- Subkultur i mikrobiologi:En trin-for-trin guide til dyrkning og isolering af mikroorganismer
- Hvad sker der, når en ukontrollerbar kraft vil ramme Immmobile -objekt?
- Når du tænder for en radio, hvad er en energiændring, der sker?
- Mørk storm på Neptun vender retningen om, muligvis kaste et fragment


