Begrænsningsreaktantberegning:Bestemmelse af Mg(OH)₂-produktion
1. Identificer den begrænsende reaktant
* Den begrænsende reaktant er den reaktant, der bliver brugt først og bestemmer den maksimale mængde produkt, der kan dannes.
* For at finde den begrænsende reaktant skal vi sammenligne reaktanternes molforhold med støkiometrien i den balancerede ligning.
* Den afbalancerede ligning viser molforholdet: 1 mol MgCl2 reagerer med 2 mol KOH.
* Vi har 3 mol MgCl₂ og 4 mol KOH.
* For at finde den begrænsende reaktant kan vi beregne, hvor mange mol KOH der skal til for at reagere fuldstændigt med 3 mol MgCl₂:
* (3 mol MgCl2) * (2 mol KOH / 1 mol MgCl2) =6 mol KOH påkrævet.
* Da vi kun har 4 mol KOH, er det den begrænsende reaktant.
2. Beregn mængden af produceret Mg(OH)₂
* Brug molforholdet fra den balancerede ligning til at beregne mol produceret Mg(OH)₂.
* Forholdet er: 2 mol KOH producerer 1 mol Mg(OH)2.
* Beregn mol Mg(OH)₂:
* (4 mol KOH) * (1 mol Mg(OH)2 / 2 mol KOH) =2 mol Mg(OH)2
Konklusion
Fordi KOH er den begrænsende reaktant, kan der kun produceres 2 mol Mg(OH)2 i denne reaktion.
Sidste artikelBegrænsningsreagensberegning:MgCl₂ + 2KOH-reaktion
Næste artikelStøkiometri af MgCl2 og KOH Reaktion:Molberegning
 Varme artikler
Varme artikler
-
 Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling
Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling -
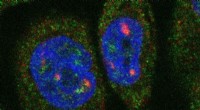 Design af lægemidler rettet mod en anden del af livets kodeIndividuelle RNA-molekyler fluorescerer inde i en brystkræftcelle. Kredit:Sunjong Kwon, Oregon Health &Science University, via Flickr De fleste lægemidler virker ved at pille ved proteiners adfærd
Design af lægemidler rettet mod en anden del af livets kodeIndividuelle RNA-molekyler fluorescerer inde i en brystkræftcelle. Kredit:Sunjong Kwon, Oregon Health &Science University, via Flickr De fleste lægemidler virker ved at pille ved proteiners adfærd -
 Forskere bruger majsstivelse til at bekæmpe skadedyrMyggen Aedes aegypti kan sprede flere sygdomme, når den rejser fra person til person. Kun hunnerne lever af blod. Denne myg er lige begyndt at spise på en persons arm. Kredit:Stephen Ausmus Tilføj
Forskere bruger majsstivelse til at bekæmpe skadedyrMyggen Aedes aegypti kan sprede flere sygdomme, når den rejser fra person til person. Kun hunnerne lever af blod. Denne myg er lige begyndt at spise på en persons arm. Kredit:Stephen Ausmus Tilføj -
 Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe
Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe


